题目内容
12.某化学兴趣小组把金属钠放到硫酸铜溶液中,实验并非如想象的有红色铜析出,而是生成一种蓝色沉淀,同学们非常好奇进行实验探究.(1)【提出问题】金属钠放到硫酸铜溶液中到底发生了怎样的化学反应?
(2)【查阅资料】钠是非常活泼的金属,能与水发生剧烈反应,并放出气体,生成的溶液显碱性
(3)【实验探究】
实验一:把一小块擦干净的金属钠放到装有少量蒸馏水的试管中,点燃生成的气体,听到“噗”的一声后燃烧起来,说明有氢气气体生成
实验二:在剩余的溶液中滴加硫酸铜溶液,发现有蓝色沉淀
(4)【实验总结】实验一中发生反应的化学方程式是2Na+2H2O=2NaOH+H2↑;实验二中发生反应的化学方程式是2NaOH+CuSO4═Cu(OH)2↓+Na2SO4
(5)【实验拓展】兴趣小组又将一小块擦干净的金属钠放入盛有FeCl3溶液的烧杯中,观察到发生了化学反应,该反应的化学方程式是6Na+2FeCl3+6H2O=3H2↑+2Fe(OH)3↓+6NaCl.
分析 (3)根据反应的物质为水和钠,结合反应前后元素的种类不变来进行解答;
(4)根据上述分析可以知道反应生成了氢氧化钠和水,可以据此写出该反应的化学方程式;
(5)根据反应原理写出反应的化学方程式解答.
解答 解:
(3)实验一根据质量守恒定律知,反应物中的元素有:Na、O、H,所以生成物中肯定含有这三种元素,而生成物中的气体能燃烧,所以该气体是氢气(H2).
(4)根据反应的物质为水和钠,结合反应前后元素的种类不变,可以知道某碱应该为氢氧化钠根据实验二的现象和钠的性质分析,钠放入硫酸铜溶液中,先与水反应生成氢氧化钠和氢气,实验一中发生反应的化学方程式是:2Na+2H2O=2NaOH+H2↑;氢氧化钠再和硫酸铜溶液反应,化学方程式为:2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(5)金属钠放入盛有FeCl3溶液的烧杯中,观察到发生了化学反应,该反应的化学方程式是:6Na+2FeCl3+6H2O=3H2↑+2Fe(OH)3↓+6NaCl
故答案是:
(3)H2;
(4)氢氧化钠(或NaOH);2Na+2H2O=2NaOH+H2↑;2NaOH+CuSO4═Cu(OH)2↓+Na2SO4.
(5)6Na+2FeCl3+6H2O=3H2↑+2Fe(OH)3↓+6NaCl
点评 解读有用信息,对操作中的描述和反应现象认真加以分析,再结合自己所学知识,此类题可迎刃而解.

练习册系列答案
相关题目
3.分类是学习和研究一种常用的科学方法.下列物质中按照单质、酸、混合物的顺序排列的是( )
| A. | 石墨 二氧化碳 石油 | B. | 氢气 硫酸 空气 | ||
| C. | 白磷 碳酸 冰水混合物 | D. | 生铁 盐酸 粗盐 |
20.现有10克CuO和ZnO的混合物,下列实验方案,不能确定CuO质量分数的是( )
| A. | 将混合物与足量H2充分反应,冷却后测出剩余固体质量 | |
| B. | 将混合物与足量CO充分反应,反应后的气体通入足量的NaOH溶液中,测出NaOH溶液质量的增加值 | |
| C. | 将混合物完全溶于稀H2SO4,加入足量铁粉,充分反应后,过滤、洗涤、干燥,测出剩余固体质量 | |
| D. | 将混合物完全溶于稀H2SO4,加入足量NaOH溶液,过滤、洗涤、干燥,测出剩余固体质量 |
17.下列实验操作中,正确的是( )
| A. | 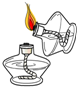 | B. |  | C. | 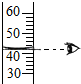 | D. | 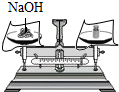 |
1.下列说法正确的是( )
| A. | 分子可以直接构成物质,则溶质都以分子形式分散到溶剂中形成溶液 | |
| B. | 中和反应生成盐和水,则生成盐和水的反应都是中和反应 | |
| C. | 铵盐能与碱反应生成氨气,则硫酸铵不能与熟石灰混合施用 | |
| D. | 一氧化碳、二氧化碳组成元素相同,则一氧化碳、二氧化碳化学性质相同 |
 已知Mg能在CO2中燃烧生成碳和一种白色固体物质,某化学兴趣小组用如图所示装置制备CO2并对Mg在CO2中燃烧生成的白色固体物质进行探究.
已知Mg能在CO2中燃烧生成碳和一种白色固体物质,某化学兴趣小组用如图所示装置制备CO2并对Mg在CO2中燃烧生成的白色固体物质进行探究.