题目内容
20.现有10克CuO和ZnO的混合物,下列实验方案,不能确定CuO质量分数的是( )| A. | 将混合物与足量H2充分反应,冷却后测出剩余固体质量 | |
| B. | 将混合物与足量CO充分反应,反应后的气体通入足量的NaOH溶液中,测出NaOH溶液质量的增加值 | |
| C. | 将混合物完全溶于稀H2SO4,加入足量铁粉,充分反应后,过滤、洗涤、干燥,测出剩余固体质量 | |
| D. | 将混合物完全溶于稀H2SO4,加入足量NaOH溶液,过滤、洗涤、干燥,测出剩余固体质量 |
分析 A.混合物与足量H2充分反应,冷却后测出剩余固体质量,可以列等式进行计算.
B.混合物在高温下通入足量CO气体,反应后的气体通入足量的NaOH溶液中,测出NaOH溶液质量的增加值(即为生成二氧化碳的质量),可列式计算.
C.氧化铜、氧化锌与稀硫酸反应分别生成硫酸铜、硫酸锌溶液,加入足量铁粉,铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,铁不与硫酸锌溶液反应,但铁粉足量,反应后有剩余,进行分析判断.
D.氧化铜、氧化锌与稀硫酸反应分别生成硫酸铜、硫酸锌溶液,加入足量NaOH溶液,分别生成氢氧化铜、氢氧化锌沉淀,测出氢氧化铜、氢氧化锌沉淀的质量,可列式计算.
解答 解:A、设CuO和ZnO的物质的量分别为xmol、ymol,则有80x+81y=10g,64x+65y=剩余固体质量,可以计算出CuO质量分数;
或者是由混合物的质量、剩余固体的质量,可以计算出混合物中氧元素的质量,进而可以计算出CuO质量分数;故选项错误.
B、混合物在高温下通入足量CO气体,反应后的气体通入足量的NaOH溶液中,测出NaOH溶液质量的增加值(即为生成二氧化碳的质量),设CuO和FeO的物质的量分别为xmol、ymol,则有80x+72y=10g,(x+y)mol×44g/mol=二氧化碳的质量,可以计算出CuO质量分数;
或者是由生成二氧化碳气体的质量,由反应的化学方程式,可以计算出混合物中氧化铜的质量;故选项错误.
C、氧化铜、氧化锌与稀硫酸反应分别生成硫酸铜、硫酸锌溶液,加入足量铁粉,铁能与硫酸铜溶液反应生成硫酸亚铁溶液和铜,铁不与硫酸锌溶液反应,但铁粉足量,反应后有剩余,无法确定生成铜的质量,不能计算出CuO质量分数,故选项正确.
D、氧化铜、氧化锌与稀硫酸反应分别生成硫酸铜、硫酸锌溶液,加入足量NaOH溶液,分别生成氢氧化铜、氢氧化锌沉淀,与A、B选项同理,可以计算出CuO质量分数,故选项错误.
故选:C.
点评 本题有一定难度,考查物质的含量的测定实验方案的设计,侧重于学生的分析能力和计算能力的考查,把握反应的原理和计算方法是正确解答本题的关键.

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案(1)为探究不同催化剂对氯酸钾分解速度的影响,甲设计以下对比实验探究,在相同温度下,比较两组实验产生O2的快慢.
Ⅰ.将3.0g KClO3与1.0g MnO2均匀混合加热
Ⅱ.将x g KClO3与1.0g CuO均匀混合加热
实验中Ⅱ中x的值应为3.0g;Ⅰ中反应的化学方程式是2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.
实验结论:在其他条件相同的情况下,MnO2的催化能力比CuO强.
(2)乙探究了影响双氧水分解速度的某种因素.实验数据记录和可选装置如表:
| 双氧水的质量 | 双氧水的浓度 | MnO2的质量 | 相同时间内产生O2体积 | |
| Ⅰ | 50.0g | 1% | 0.1g | 9mL |
| Ⅱ | 50.0g | 2% | 0.1g | 16mL |
| Ⅲ | 50.0g | 4% | 0.1g | 31mL |
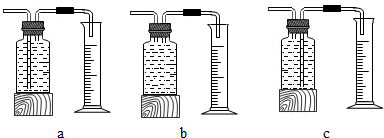
本实验中,测量O2体积的装置应该是C(填编号);
实验结论:乙探究中,在其他条件相同的情况下,双氧水的浓度越大,双氧水分解得越快.
| A. | 氢氧化钠能和酸反应,生活中可用氢氧化钠治疗胃酸过多 | |
| B. | 气体分子间间隔大,6000L氧气加压可装入40L的钢瓶中 | |
| C. | 浓硫酸具有吸水性,可用作干燥剂 | |
| D. | 洗洁精有乳化功能,能洗去碗筷上的油污 |
| A. | 丙氨酸由碳、氢、氧、氮四种元素组成 | |
| B. | 一个丙氨酸分子中含有13个原子 | |
| C. | 丙氨酸的相对分子质量为89 | |
| D. | 丙氨酸中氧元素与氮元素的质量比为2:1 |
【提出问题】该烧杯中溶液的溶质是什么?
【猜想】猜想一:只有CaCl2;猜想二:CaCl2和HCl;猜想三:含有CaCl2和Ca(OH)2;猜想四:含有
CaCl2、HCl和Ca(OH)2.
同学们讨论后一致认为猜想四不合理,理由是稀盐酸与氢氧化钙在溶液中不能共存.
【查阅资料】氯化钙溶液呈中性
【进行实验】同学们设计可如下不同的实验方案,证明猜想二是成立的.请你帮他们填写有关实验步骤或实验现象.
| 方案 | 实验步骤 | 实验现象 |
| 方案一 | 取少量溶液于试管中,滴加紫色石蕊溶液 | 紫色石蕊溶液变红色 |
| 方案二 | 取少量氧化铜粉末于试管中,加入一定量的烧杯中的溶液 | 黑色粉末逐渐溶解,溶液变蓝色 |
| 方案三 | 取少量烧杯内溶液于另一支试管中,加入碳酸钠溶液等 | 产生气泡 |
要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的碳酸钙,然后过滤,该除杂原理用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑.
| A. | 冰雪融化 | B. | 白酒挥发 | C. | 森林失火 | D. | 树枝折断 |
