题目内容
17.下列实验操作中,正确的是( )| A. | 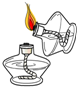 | B. |  | C. | 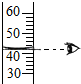 | D. | 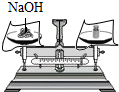 |
分析 A、点燃酒精灯时,应用火柴点燃.图中操作错误会引起安全事故;
B、运用稀释浓硫酸时不能将水倒入浓硫酸中要将浓硫酸倒入水中解答;
C、量取液体时,视线与液体的凹液面最低处保持水平;
D、根据氢氧化钠有腐蚀性进行分析.
解答 解:A、点燃酒精灯时,用火柴点燃,如果用燃着的酒精灯去点燃另一个酒精灯,会引起酒精失火,造成危险,故A错误;
B、稀释浓硫酸时不能将水倒入浓硫酸中要将浓硫酸倒入水中,防止水浮在浓硫酸的水面上沸腾溅出,B操作不正确;
C、量取液体时,视线与液体的凹液面最低处保持水平.图示正确;
D、氢氧化钠具有腐蚀性,称量时应放在玻璃器皿中,不能放在纸上,防止腐蚀托盘,故错误;
故选C.
点评 本题难度不大,熟悉各种仪器的用途及使用注意事项、掌握常见化学实验基本操作的注意事项是解答此类试题的关键.

练习册系列答案
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案
相关题目
7.BGO是我国研制的一种闪烁晶体材料,曾用于诺贝尔获奖得者丁肇中的著名实验.BGOS是锗酸铋(化学式为Bi4GO3O12)的简称.已知在BGO中锗(Ge)的化合价与GeO2中锗的化合价相等,则在BGO中铋(Bi)的化合价为( )
| A. | +5 | B. | +4 | C. | +3 | D. | +2 |
8.蛋白质时人类重要的营养物质,它是由多种氨基酸构成的化合物,丙氨酸(C3H7O2N)是其中一种,下列有关丙氨酸的叙述不正确的是( )
| A. | 丙氨酸由碳、氢、氧、氮四种元素组成 | |
| B. | 一个丙氨酸分子中含有13个原子 | |
| C. | 丙氨酸的相对分子质量为89 | |
| D. | 丙氨酸中氧元素与氮元素的质量比为2:1 |
5.某实验小组的同学在做酸碱中和反应的实验时,向烧杯中的氢氧化钙溶液中加入一定量的稀盐酸后,发现忘记了滴加酸碱指示剂.因此,他们停止滴加稀盐酸,并对烧杯中溶液的溶质成分进行探究.
【提出问题】该烧杯中溶液的溶质是什么?
【猜想】猜想一:只有CaCl2;猜想二:CaCl2和HCl;猜想三:含有CaCl2和Ca(OH)2;猜想四:含有
CaCl2、HCl和Ca(OH)2.
同学们讨论后一致认为猜想四不合理,理由是稀盐酸与氢氧化钙在溶液中不能共存.
【查阅资料】氯化钙溶液呈中性
【进行实验】同学们设计可如下不同的实验方案,证明猜想二是成立的.请你帮他们填写有关实验步骤或实验现象.
【反思交流】
要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的碳酸钙,然后过滤,该除杂原理用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑.
【提出问题】该烧杯中溶液的溶质是什么?
【猜想】猜想一:只有CaCl2;猜想二:CaCl2和HCl;猜想三:含有CaCl2和Ca(OH)2;猜想四:含有
CaCl2、HCl和Ca(OH)2.
同学们讨论后一致认为猜想四不合理,理由是稀盐酸与氢氧化钙在溶液中不能共存.
【查阅资料】氯化钙溶液呈中性
【进行实验】同学们设计可如下不同的实验方案,证明猜想二是成立的.请你帮他们填写有关实验步骤或实验现象.
| 方案 | 实验步骤 | 实验现象 |
| 方案一 | 取少量溶液于试管中,滴加紫色石蕊溶液 | 紫色石蕊溶液变红色 |
| 方案二 | 取少量氧化铜粉末于试管中,加入一定量的烧杯中的溶液 | 黑色粉末逐渐溶解,溶液变蓝色 |
| 方案三 | 取少量烧杯内溶液于另一支试管中,加入碳酸钠溶液等 | 产生气泡 |
要使烧杯内溶液的溶质只含CaCl2,需要除去杂质,其中的一种方法是向烧杯中加入过量的碳酸钙,然后过滤,该除杂原理用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑.
9.下列变化属于化学变化的是( )
| A. | 冰雪融化 | B. | 白酒挥发 | C. | 森林失火 | D. | 树枝折断 |
17.氧化钙和碳酸钙的固体混合物质量为100g,将其高温煅烧至碳酸钙完全分解,称得剩余固体的质量为70g.则原固体混合物中钙元素的质量分数为( )
| A. | 20% | B. | 40% | C. | 50% | D. | 70% |