题目内容
完成下列变化的化学方程式,并按要求填空.
(1)宇宙飞船上利用氢气、氧气在催化剂作用下反应作燃料电池: ;该反应中氢气和氧气的体积比为 .
(2)二氧化碳气体通过炽热的碳层: ;其基本反应类型是 .
(3)如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量的水冲洗,然后涂上3%~5%的NaHCO3溶液: ;说明NaHCO3溶液呈 (选填“酸性”、“中性”或“碱性”).
(4)少量硫酸铵固体与熟石灰混合研磨: ;检验该气体可用 试纸.
(5)受到猛烈撞击时,硝酸铵会迅速分解生成一氧化二氮气体和另一种氧化物: ;一氧化二氮中氮元素的化合价为 .
(1)宇宙飞船上利用氢气、氧气在催化剂作用下反应作燃料电池:
(2)二氧化碳气体通过炽热的碳层:
(3)如果不慎将浓硫酸沾到皮肤或衣服上,应立即用大量的水冲洗,然后涂上3%~5%的NaHCO3溶液:
(4)少量硫酸铵固体与熟石灰混合研磨:
(5)受到猛烈撞击时,硝酸铵会迅速分解生成一氧化二氮气体和另一种氧化物:
考点:书写化学方程式、文字表达式、电离方程式,常见气体的检验与除杂方法,有关元素化合价的计算,反应类型的判定
专题:化学用语和质量守恒定律
分析:首先根据反应原理找出反应物、生成物、反应条件,根据化学方程式的书写方法、步骤进行书写即可.
解答:解:(1)氢气在催化剂作用下反应生成水,反应的化学方程式是为:2H2+O2
2H2O;该反应中氢气和氧气的体积比为2:1.
(2)二氧化碳气体通过炽热的碳层生成一氧化碳,反应的化学方程式是为:C+CO2
2CO;该反应符合“多变一”的特征,属于化合反应.
(3)NaHCO3溶液与硫酸反应生成硫酸钠、水和二氧化碳,反应的化学方程式是为:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O;说明NaHCO3溶液呈碱性.
(4)硫酸铵固体与熟石灰混合研磨生成硫酸钙、水和二氧化碳,反应的化学方程式是为:(NH4)2SO4+Ca(OH)2═CaSO4+2NH3↑+2H2O;生成的氨气可用湿润的红色石蕊试纸检验,若变蓝,说明是氨气.
(5)受到猛烈撞击时,硝酸铵会迅速分解生成一氧化二氮气体和另一种氧化物;由质量守恒定律,化学反应中元素的种类不变,反应物中含有氢元素,因此另一种氧化物中应该含有氢元素,所以含氢元素的氧化物是水;该反应的化学方程式为:NH4NO3
N2O↑+2H2O.
氧元素显-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)=0,则x=+1价.
故答案为:(1)2H2+O2
2H2O;2:1;
(2)C+CO2
2CO;化合反应;
(3)2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O;碱性;
(4)(NH4)2SO4+Ca(OH)2═CaSO4+2NH3↑+2H2O;湿润的红色石蕊;
(5)NH4NO3
N2O↑+2H2O;+1.
| ||
(2)二氧化碳气体通过炽热的碳层生成一氧化碳,反应的化学方程式是为:C+CO2
| ||
(3)NaHCO3溶液与硫酸反应生成硫酸钠、水和二氧化碳,反应的化学方程式是为:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O;说明NaHCO3溶液呈碱性.
(4)硫酸铵固体与熟石灰混合研磨生成硫酸钙、水和二氧化碳,反应的化学方程式是为:(NH4)2SO4+Ca(OH)2═CaSO4+2NH3↑+2H2O;生成的氨气可用湿润的红色石蕊试纸检验,若变蓝,说明是氨气.
(5)受到猛烈撞击时,硝酸铵会迅速分解生成一氧化二氮气体和另一种氧化物;由质量守恒定律,化学反应中元素的种类不变,反应物中含有氢元素,因此另一种氧化物中应该含有氢元素,所以含氢元素的氧化物是水;该反应的化学方程式为:NH4NO3
| ||
氧元素显-2价,设氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:2x+(-2)=0,则x=+1价.
故答案为:(1)2H2+O2
| ||
(2)C+CO2
| ||
(3)2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O;碱性;
(4)(NH4)2SO4+Ca(OH)2═CaSO4+2NH3↑+2H2O;湿润的红色石蕊;
(5)NH4NO3
| ||
点评:本题难度不大,考查学生根据反应原理书写化学方程式的能力,化学方程式书写经常出现的错误有不符合客观事实、不遵守质量守恒定律、不写条件、不标符号等.

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案 暑假作业安徽少年儿童出版社系列答案
暑假作业安徽少年儿童出版社系列答案
相关题目
下列有关实验现象描述错误的是( )
| A、红磷在空气中燃烧产生大量白烟 |
| B、铁丝浸入硫酸铜溶液中,有红色物质析出 |
| C、镁条在空气中燃烧,发出耀眼白光 |
| D、打开浓盐酸的试剂瓶盖,瓶口有白烟产生 |

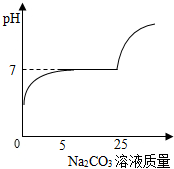 某同学将为了测定实验室制取二氧化碳后的废液中的成分及含量,他将废液过滤,然后取滤液10.0g,向其中滴加10.6%的碳酸钠溶液,并测定溶液的pH,绘制图象如图:
某同学将为了测定实验室制取二氧化碳后的废液中的成分及含量,他将废液过滤,然后取滤液10.0g,向其中滴加10.6%的碳酸钠溶液,并测定溶液的pH,绘制图象如图:

 如图是A、B、C三种物质的溶解度曲线,请据图回答:
如图是A、B、C三种物质的溶解度曲线,请据图回答: