题目内容
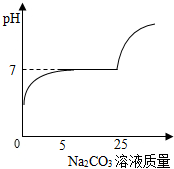 某同学将为了测定实验室制取二氧化碳后的废液中的成分及含量,他将废液过滤,然后取滤液10.0g,向其中滴加10.6%的碳酸钠溶液,并测定溶液的pH,绘制图象如图:
某同学将为了测定实验室制取二氧化碳后的废液中的成分及含量,他将废液过滤,然后取滤液10.0g,向其中滴加10.6%的碳酸钠溶液,并测定溶液的pH,绘制图象如图:(1)曲线中有一段与X轴平行的原因
(2)计算废液中氯化钙的溶质质量分数(可能用到的相对原子质量:
Ca:40,Cl:35.5,Na:23,C:12,O:16.)
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:由图象知,一开始溶液的pH<7,故废液中含有盐酸和氯化钙,加入5克碳酸钠前溶液呈酸性,加入25克碳酸钠后因碳酸钠过量且碳酸钠显碱性,但在5克和25克间是碳酸钠与氯化钙反应生产的氯化钠是中性故保持PH为7不变,故可根据与氯化钙反应的碳酸钠的质量计算氯化钙的质量,进而求质量分数.
解答:解:(1)废液中含有盐酸,加入5克碳酸钠前溶液呈酸性,加入25克碳酸钠后因碳酸钠过量且碳酸钠显碱性,但在5克和25克间是碳酸钠与氯化钙反应生产的氯化钠是中性故保持PH为7不变;
(2)设废液中氯化钙的质量为x,经分析实际和氯化钙反应的碳酸钠溶液的质量为20克
CaCl2+Na2CO3=CaCO3↓+2NaCl
111 106
x 20g×10.6%
=
x=2.22g
废液中氯化钙的溶质质量分数:
×100%=22.2%
答:废液中氯化钙的溶质质量分数为22.2%.
(2)设废液中氯化钙的质量为x,经分析实际和氯化钙反应的碳酸钠溶液的质量为20克
CaCl2+Na2CO3=CaCO3↓+2NaCl
111 106
x 20g×10.6%
| 111 |
| x |
| 106 |
| 20g×10.6% |
x=2.22g
废液中氯化钙的溶质质量分数:
| 2.22g |
| 10g |
答:废液中氯化钙的溶质质量分数为22.2%.
点评:会正确分析图象是正确解决本题的关键.

练习册系列答案
相关题目
下面是小青同学对部分化学知识的归纳,其中正确的一组是( )
| A、实验记录:①用10mL量筒量取7.025mL水;②用托盘天平称取5.6g氯化钠 |
| B、安全常识:①酒精灯打翻起火,用湿抹布扑灭;②冬用煤炉取暖,应保证室内通风 |
| C、化学与健康:①人体缺维生素A会引起夜盲症;②禁止使用任何食品添加剂 |
| D、化学与生活:①用钢丝球擦洗铝锅上的污垢;②用食醋除水垢 |
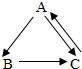 A、B、C是初中常见的三种白色固体,它们的转化关系如右图所示(部分物质已略去),其中A的相对分子质量为100,B是常用的干燥剂,C是氯化物.请写出B的俗名
A、B、C是初中常见的三种白色固体,它们的转化关系如右图所示(部分物质已略去),其中A的相对分子质量为100,B是常用的干燥剂,C是氯化物.请写出B的俗名