题目内容
8.我县某中学化学兴趣小组的同学欲除去固体氯化钠中混有的氯化钙.该小组同学设计的方案如下,请你参与实验并回答问题.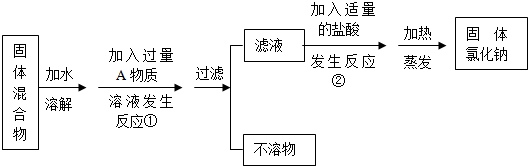
(1)写出A物质的化学式Na2CO3,写出反应①的化学方程式Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)写出反②应的化学方程式Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)反应②中如果加入的盐酸也过量,则对所得到的氯化钠的纯度没有(填“有”或“没有”)影响.
分析 氯化钙能和碳酸钠反应生成白色沉淀碳酸钙和氯化钠;
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳;
盐酸易挥发,加热含有盐酸的氯化钠溶液时,随着水的蒸发,氯化氢气体也随着挥发,当水完全蒸发后,氯化氢也完全挥发.
解答 解:(1)氯化钠和氯化钙的混合溶液中,加入碳酸钠时,氯化钠不能和碳酸钠反应,氯化钙能和碳酸钠反应,因此利用碳酸钠可以除去溶液中的氯化钙,即加入的A是碳酸钠,碳酸钠的化学式是Na2CO3;
氯化钙能和碳酸钠反应生成白色沉淀碳酸钙和氯化钠,反应的化学方程式为:Na2CO3+CaCl2═CaCO3↓+2NaCl.
故填:Na2CO3;Na2CO3+CaCl2═CaCO3↓+2NaCl.
(2)碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,因此加入稀盐酸能够除去过量的碳酸钠,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
(3)由于盐酸易挥发,反应②中如果加入的盐酸也过量,随着水的蒸发,氯化氢气体也随着挥发,当水完全蒸发后,氯化氢也完全挥发,因此对所得到的氯化钠的纯度没有影响.
故填:没有.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
18.某学生的实验报告中有以下实验数据,其中正确的是( )
| A. | 用托盘天平称取2.5g锌 | B. | 用量筒量取5.29mL盐酸 | ||
| C. | 用pH试纸测得某溶液的pH是5.4 | D. | 用托盘天平称取2.542g食盐 |
19.请你按酸、碱、氧化物的顺序排列,下列排序正确的是( )
| A. | H2SO4、MgO、NaOH | B. | H2O、Ca(OH)2、HCl | ||
| C. | H2SO4、NaOH、Al2O3 | D. | KOH、HNO3、CO2 |
13.下列物质中,不属于氧化物的是( )
| A. | Al2O3 | B. | H2O2 | C. | KMnO4 | D. | Na2O2 |