题目内容
18.某学生的实验报告中有以下实验数据,其中正确的是( )| A. | 用托盘天平称取2.5g锌 | B. | 用量筒量取5.29mL盐酸 | ||
| C. | 用pH试纸测得某溶液的pH是5.4 | D. | 用托盘天平称取2.542g食盐 |
分析 A、根据托盘天平的精确度考虑;B、根据量筒的精确度考虑;C、根据pH试纸测得的数值的特点考虑;D、根据托盘天平的精确度考虑.
解答 解:A、托盘天平只能准确到0.1g,所以能用托盘天平称取2.5g锌,故A正确;
B、根据所量取液体量可知需要10毫升量筒即可,所以只能准确到0.1毫升,故B错误;
C、由于pH试纸上的数只有整数,所以测得溶液的pH只能准确到整数,不能到小数,故C错;
D、托盘天平只能准确到0.1g,所以不能用托盘天平称取2.542g食盐,故D错.
故选A.
点评 通过回答本题要知道托盘天平只能准确到0.1g,pH试纸测得溶液的pH只能准确到整数,量筒不能准确到小数点后两位小数.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
6.下列物质间不能发生置换反应的是( )
| A. | Cu和FeCl2 | B. | Mg和浓盐酸 | C. | Zn和CuSO4 | D. | Al和稀硫酸 |
13.下列溶液,能使紫色石蕊试液变红的是( )
| A. | 石灰水 | B. | 食盐水 | C. | 盐酸 | D. | 氢氧化钠溶液 |
10.漂白粉的主要成分为次氯酸钙[Ca(ClO)2]和氯化钙,即可用作漂白剂,又可用作消毒剂.漂白粉中有效成分是[Ca(ClO)2],漂白的原理是:Ca(ClO)2在空气中发生反应Ca(ClO)2+CO2+H2O=CaCO3↓+2HClO;HClO是一种酸性比盐酸弱的酸,不稳定,具有漂白性,能使品红等有色物质褪色.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小 (填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2+2HCl=CaCl2+2HClO.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
(1)漂白粉是一种混合物(填“纯净物”或“混合物”).
(2)HClO在常温下分解,反应为2HClO=2HCl+O2↑.某瓶HClO溶液放置一段时间后,溶液的pH减小 (填“增大”或“减小”或“不变”).
(3)在漂白粉中滴加盐酸,能加快漂白的速率.写出漂白粉中加入盐酸反应的化学方程式Ca(ClO)2+2HCl=CaCl2+2HClO.
(4)有一包长时间放置的漂白粉,想知道该漂白粉是否变质,某同学设计了下列探究实验.
【提出问题】长时间放置的漂白粉是否变质?
【猜 想】
猜想1:该漂白粉未变质,固体成分为CaCl2、Ca(ClO)2;
猜想2:该漂白粉部分变质,固体成分为CaCl2、Ca(ClO)2、CaCO3;
猜想3:该漂白粉全部变质,固体成分为CaCl2、CaCO3.
【实验探究】限选试剂及仪器:盐酸、石灰水、品红溶液、试管、带导管的单孔塞.
| 实验操作 | 实验现象 | 实验结论 |
| 1①取少量样品于试管中,加入适量稀盐酸,塞上带导管的单孔塞,把导管插入另一试管里的石灰水中. | 有气体产生,气体使石灰水变浑浊. | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液. | 品红溶液褪色. |
7.化学是一门以实验为基础的科学.下列有关实验现象的描述中不正确的是( )
| A. | 在滴有酚酞的盐酸中逐滴加入氧氧化钠溶液,溶液颜色由无色逐渐变成红色 | |
| B. | 红磷在空气中燃烧,产生大量白色烟雾 | |
| C. | 细铁丝在氧气中剿烈燃烧,火星四射,有黑色固体生成 | |
| D. | 少量高锰酸钾固体溶于水可得到紫红色溶液 |
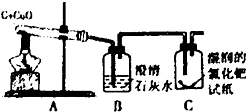 李洋同学在实验室用木炭和氧化铜两种黑色粉末在高温下反应制取单质铜,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ 他联想到单质碳的一些化学性质,认为在该实验中还可能会有CO产生.
李洋同学在实验室用木炭和氧化铜两种黑色粉末在高温下反应制取单质铜,反应的化学方程式为:C+2CuO$\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑ 他联想到单质碳的一些化学性质,认为在该实验中还可能会有CO产生.