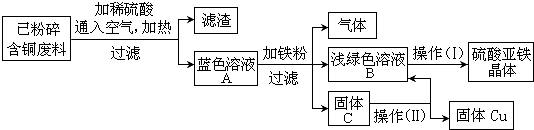
题目内容
17. 某化学兴趣小组在做完用石灰石和稀盐酸制取二氧化碳的实验后,对反应后的剩余溶液的溶质成分产生了兴趣,他们进行了以下实验探究.
某化学兴趣小组在做完用石灰石和稀盐酸制取二氧化碳的实验后,对反应后的剩余溶液的溶质成分产生了兴趣,他们进行了以下实验探究.【提出猜想】实验室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,根据反应原理,小组成员进行了如下猜想.
猜想一:只有CaCl2; 猜想二:CaCl2和HCl.
【实验探究】为了验证猜想,该兴趣小组的同学设计了如图表实验方案.
| 方案编号 | 方案1 | 方案2 | 方案3 |
| 实验操作 (分别取少量实验后的溶液于试管中) |  |  |  |
| 实验现象 | 对照标准比色卡: pH<7. | 产生白色沉淀. | 先有气体产生,后有白色沉淀生成. |
| 实验结论 | 猜想二成立. | ||
①“实验操作”中的错误是pH试纸浸入溶液中.
②“实验方案”中也有一个错误的,错误的原因是AgNO3与CaCl2反应也会生成白色沉淀,不能证明一定有HCl存在.
(2)该兴趣小组的小华同学观察到反应后容器内有少量固体剩余,得出溶液中肯定没有盐酸的结论,其他同学认为小华的说法不合理,其理由是剩余固体可能是石灰石中的杂质.
【拓展延伸】
(1)该兴趣小组的小华同学准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示,求该Na2CO3溶液中溶质的质量分数.
(2)为节约资源和避免实验废液对环境的污染,该兴趣小组的同学想从剩余溶液中得到尽可能多的氯化钙固体,同学们一致认为加入稍过量的CaCO3(填化学式),经过滤、蒸发等操作后即可完成.
分析 根据已有的知识进行分析解答,制取二氧化碳可以使用碳酸钙和盐酸反应生成氯化钙、水和二氧化碳;根据实验操作的注意实现结合图示、以及物质的性质和物质间反应的实验现象进行解答.
解答 解:【提出猜想】碳酸钙能与盐酸反应生成氯化钙、水和二氧化碳,故填:CaCO3+2HCl═CaCl2+H2O+CO2↑;
【实验探究】盐酸能与碳酸钠反应生成二氧化碳气体,碳酸钠能与氯化钙反应生成碳酸钙沉淀,故会观察到先有气体产生,后有白色沉淀生成,故填:先有气体产生,后有白色沉淀生成;
【评价反思】
(1)①据图可以看出,操作中的错误是pH试纸浸入溶液中,故填:pH试纸浸入溶液中;
②即使没有盐酸,AgNO3与CaCl2反应也会生成白色沉淀,不能证明一定有HCl存在,故填:AgNO3与CaCl2反应也会生成白色沉淀,不能证明一定有HCl存在;
(2)石灰石是混合物,剩余固体可能是石灰石中的杂质,故填:剩余固体可能是石灰石中的杂质;
【拓展延伸】
(1)解:设20g碳酸钠溶液中溶质的质量为X
Na2CO3+CaCl2═CaCO3↓+2NaCl
106 100
X 5g
$\frac{106}{100}=\frac{X}{5g}$
X=5.3g
Na2CO3%=$\frac{5.3g}{20g}$×100%=26.5%
答:该Na2CO3溶液中溶质的质量分数为26.5%.
(2)想从剩余溶液中得到尽可能多的氯化钙固体可以加入稍过量的碳酸钙,故填:CaCO3.
点评 本题考查的是剩余物质成分的探究,完成此题,可以依据已有的物质的性质进行.

练习册系列答案
相关题目
11. 将燃着的镁带伸入二氧化碳气体中,镁带继续剧烈燃烧,生成氧化镁和碳.下列叙述错误的是( )
将燃着的镁带伸入二氧化碳气体中,镁带继续剧烈燃烧,生成氧化镁和碳.下列叙述错误的是( )
 将燃着的镁带伸入二氧化碳气体中,镁带继续剧烈燃烧,生成氧化镁和碳.下列叙述错误的是( )
将燃着的镁带伸入二氧化碳气体中,镁带继续剧烈燃烧,生成氧化镁和碳.下列叙述错误的是( )| A. | 一定条件下CO2有助燃性 | |
| B. | 反应的化学方程式为:2Mg+CO2$\underline{\underline{点燃}}$2MgO+C | |
| C. | 一定条件下CO2有可燃性 | |
| D. | 镁着火时不能用二氧化碳扑灭 |
8.已知在铁制品上连接比铁活泼的金属是防止铁生锈的方法之一.下列金属可按此方法用于铁制品防锈的是( )
| A. | Ag | B. | Pb(铅) | C. | Cu | D. | Zn |
5.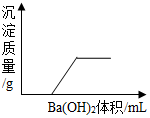 有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
 有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )
有一溶液是由盐酸、硫酸、硫酸铁、氯化铁、稀硝酸、硝酸铁几种中的两种混合而成,向该溶液中加Ba(OH)2溶液的体积与生成沉淀的质量关系如图所示,则该溶液是( )| A. | 硝酸、硝酸铁 | B. | 硫酸、氯化铁 | C. | 盐酸、氯化铁 | D. | 盐酸、硫酸铁 |
2.某样化学兴趣小组的同学在实验室发现一盛石灰水的试剂瓶,瓶壁和瓶塞周围有一些白色粉末.为了弄清楚白色粉末的成分及形成原因,他们进行了如下探究:
【提出问题】白色粉末成分的猜想和成因分析.
【作出猜想】猜想Ⅰ:可能是CaCO3;原因是石灰水与空气中的CO2反应.
猜想Ⅱ:可能是Ca(OH)2 ;原因是溶剂蒸发,石灰水中的溶质结晶析出.
猜想Ⅲ:还可能是Ca(OH)2和CaCO3;原因是石灰水会与空气中的CO2反应,且溶剂蒸发时,石灰水中的溶质会结晶析出.
【实验探究】甲同学取白色粉末于试管中,加少量的水振荡,发现试管底部有白色固体.于是他得出白色固体粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了如表所示实验,请完成实验报告:
由上述实验可知,猜想Ⅲ是正确的.
【拓展反思】通过上述实验的探究,同学们向实验员提出了保存易变质溶液的下列建议,合理的是ab.
a、密封保存 b、使用前临时配制 c、禁止使用该试剂.
【提出问题】白色粉末成分的猜想和成因分析.
【作出猜想】猜想Ⅰ:可能是CaCO3;原因是石灰水与空气中的CO2反应.
猜想Ⅱ:可能是Ca(OH)2 ;原因是溶剂蒸发,石灰水中的溶质结晶析出.
猜想Ⅲ:还可能是Ca(OH)2和CaCO3;原因是石灰水会与空气中的CO2反应,且溶剂蒸发时,石灰水中的溶质会结晶析出.
【实验探究】甲同学取白色粉末于试管中,加少量的水振荡,发现试管底部有白色固体.于是他得出白色固体粉末是CaCO3的结论.乙同学认为甲同学的结论不严密,理由是Ca(OH)2微溶于水.
为了得出较严密的结论,他们进行了如表所示实验,请完成实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ?取上述试管中的上层清液,滴加1─2滴无色酚酞试液 | 溶液呈红色 | 白色粉末中含有Ca(OH)2 |
| ?往上述试管残留的白色固体中滴加稀盐酸 | 有气泡产生 | 白色粉末中含CaCO3 |
【拓展反思】通过上述实验的探究,同学们向实验员提出了保存易变质溶液的下列建议,合理的是ab.
a、密封保存 b、使用前临时配制 c、禁止使用该试剂.
9.区别纯净水和过氧化氢溶液最简便的方法是( )
| A. | 滴入澄清石灰水,观察是否浑浊 | |
| B. | 将带火星小木条伸入,观察是否复燃 | |
| C. | 加入MnO2,观察是否产生气泡 | |
| D. | 将燃着的小木条伸入,观察是否更旺 |
7.原子核内有6个质子和6个中子的一种碳原子的质量为x g,另一种元素R的原子质量为 y g.则R的相对原子质量为( )
| A. | y g | B. | $\frac{12x}{y}$g | C. | $\frac{y}{x}$ | D. | $\frac{12y}{x}$ |