题目内容
7.原子核内有6个质子和6个中子的一种碳原子的质量为x g,另一种元素R的原子质量为 y g.则R的相对原子质量为( )| A. | y g | B. | $\frac{12x}{y}$g | C. | $\frac{y}{x}$ | D. | $\frac{12y}{x}$ |
分析 根据某原子的相对原子相对质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,结合题意进行分析解答即可.
解答 解:已知原子核内有6个质子和6个中子的碳原子质量为x克,若另一种原子的质量为y克,则另一种原子的相对原子质量为$\frac{yg}{xg×\frac{1}{12}}$=$\frac{12y}{x}$.
故选:D.
点评 本题难度不大,掌握原子的相对原子相对质量=$\frac{该元素的一个原子的质量}{一种碳原子质量×\frac{1}{12}}$,并能灵活运用是正确解答本题的关键

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
17. 某化学兴趣小组在做完用石灰石和稀盐酸制取二氧化碳的实验后,对反应后的剩余溶液的溶质成分产生了兴趣,他们进行了以下实验探究.
某化学兴趣小组在做完用石灰石和稀盐酸制取二氧化碳的实验后,对反应后的剩余溶液的溶质成分产生了兴趣,他们进行了以下实验探究.
【提出猜想】实验室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,根据反应原理,小组成员进行了如下猜想.
猜想一:只有CaCl2; 猜想二:CaCl2和HCl.
【实验探究】为了验证猜想,该兴趣小组的同学设计了如图表实验方案.
【评价反思】(1)老师对同学们能用多种方法进行探究,并且得出正确结论给予肯定,同时指出【实验探究】中存在两处明显错误,请大家反思.同学们经过反思发现了这两处错误:
①“实验操作”中的错误是pH试纸浸入溶液中.
②“实验方案”中也有一个错误的,错误的原因是AgNO3与CaCl2反应也会生成白色沉淀,不能证明一定有HCl存在.
(2)该兴趣小组的小华同学观察到反应后容器内有少量固体剩余,得出溶液中肯定没有盐酸的结论,其他同学认为小华的说法不合理,其理由是剩余固体可能是石灰石中的杂质.
【拓展延伸】
(1)该兴趣小组的小华同学准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示,求该Na2CO3溶液中溶质的质量分数.
(2)为节约资源和避免实验废液对环境的污染,该兴趣小组的同学想从剩余溶液中得到尽可能多的氯化钙固体,同学们一致认为加入稍过量的CaCO3(填化学式),经过滤、蒸发等操作后即可完成.
 某化学兴趣小组在做完用石灰石和稀盐酸制取二氧化碳的实验后,对反应后的剩余溶液的溶质成分产生了兴趣,他们进行了以下实验探究.
某化学兴趣小组在做完用石灰石和稀盐酸制取二氧化碳的实验后,对反应后的剩余溶液的溶质成分产生了兴趣,他们进行了以下实验探究.【提出猜想】实验室制取二氧化碳的化学方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,根据反应原理,小组成员进行了如下猜想.
猜想一:只有CaCl2; 猜想二:CaCl2和HCl.
【实验探究】为了验证猜想,该兴趣小组的同学设计了如图表实验方案.
| 方案编号 | 方案1 | 方案2 | 方案3 |
| 实验操作 (分别取少量实验后的溶液于试管中) |  |  |  |
| 实验现象 | 对照标准比色卡: pH<7. | 产生白色沉淀. | 先有气体产生,后有白色沉淀生成. |
| 实验结论 | 猜想二成立. | ||
①“实验操作”中的错误是pH试纸浸入溶液中.
②“实验方案”中也有一个错误的,错误的原因是AgNO3与CaCl2反应也会生成白色沉淀,不能证明一定有HCl存在.
(2)该兴趣小组的小华同学观察到反应后容器内有少量固体剩余,得出溶液中肯定没有盐酸的结论,其他同学认为小华的说法不合理,其理由是剩余固体可能是石灰石中的杂质.
【拓展延伸】
(1)该兴趣小组的小华同学准备将反应后的废液倒进废液缸时,发现实验桌上有一瓶未知质量分数的Na2CO3溶液,他决定利用该废液,测定Na2CO3溶液中溶质的质量分数.他将废液过滤,然后向废液中慢慢滴加Na2CO3溶液,加入Na2CO3溶液的质量与生成沉淀质量的关系如图所示,求该Na2CO3溶液中溶质的质量分数.
(2)为节约资源和避免实验废液对环境的污染,该兴趣小组的同学想从剩余溶液中得到尽可能多的氯化钙固体,同学们一致认为加入稍过量的CaCO3(填化学式),经过滤、蒸发等操作后即可完成.
12.为了测定硫酸铜晶体(CuSO4•XH2O)中的结晶水的含量,做下列实验,将硫酸铜晶体放
在坩埚里加热,至不含结晶水测得数据见右表
(1)反应生成水9克
(2)硫酸铜晶体中结晶水的含量的百分比为36%(CuSO4•xH2O=CuSO4+XH2O)
(3)在CuSO4•XH2O中,X=5.
| 物质 | 质量(克) |
| 坩埚+硫酸铜晶体 | 45.5 |
| 坩埚+无水硫酸铜 | 36.5 |
| 坩埚 | 20.5 |
(1)反应生成水9克
(2)硫酸铜晶体中结晶水的含量的百分比为36%(CuSO4•xH2O=CuSO4+XH2O)
(3)在CuSO4•XH2O中,X=5.
17.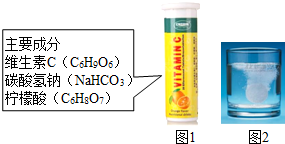 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2.
小明说:不可能含有N2,因为反应物中不含有氮元素.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
【得出结论】
(1)由实验①可知,该气体中肯定含有CO2.
(2)由实验②不能确定该气体中不含氧气.理由是即使气体中含有氧气,那么在二氧化碳存在时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
 某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.
某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2).该小组同学进行如下探究.探究一:该气体的成分.
【猜想与假设】小华说:该气体可能是CO2、O2、CO、H2、N2.
小明说:不可能含有N2,因为反应物中不含有氮元素.
小芳说:不可能含有CO和H2,因为从药品安全角度考虑,H2易燃易爆,CO有毒;
该小组同学认为:该气体可能含有CO2、O2中的一种或两种.
【进行实验】
| 实验编号 | 实验操作 | 实验现象 |
| ① | 将气体通入澄清的石灰水中 | 澄清石灰水变浑浊 |
| ② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(1)由实验①可知,该气体中肯定含有CO2.
(2)由实验②不能确定该气体中不含氧气.理由是即使气体中含有氧气,那么在二氧化碳存在时,带火星的木条也不能复燃.
探究二:维C泡腾片溶液的酸碱性.
向维C泡腾片溶液中滴加石蕊试液,溶液变红,说明溶液显酸性.
 溶解度是解决溶液相关问题的重要依据.根据如图解决下列问题:(M,N均不含结晶水)
溶解度是解决溶液相关问题的重要依据.根据如图解决下列问题:(M,N均不含结晶水)