题目内容
9. 根据表中五种气体在标准状况下的密度和溶解性,回答下列问题:
根据表中五种气体在标准状况下的密度和溶解性,回答下列问题:| 空气 | 氨气 | 甲烷 | 氯化氢 | 氧气 | |
| 密度/g•L-1 | 1.293 | 0.77l | 0.717 | 1.629 | 1.43 |
| 溶解性 | -- | 极易溶 | 难溶 | 极易溶 | 难溶 |
(2)标准状况下气体氨气的密度比空气小(填“大”或“小”);
(3)用如图所示盛满水的集气瓶收集氧气,气体应从b(填“a”或“b”)端进入.
分析 (1)根据气体的密度与水溶性答题;
(2)根据表格中的数据可以直接填空;
(3)根据氧气的性质和装置的特点进行分析填空.
解答 解:(1)能用排水法说明该气体不易溶于水或难溶于水,又能用向上排空气法收集说明该气体密度比空气密度大,所以所给气体中只有氧气;
(2)由表格中的数据得到:空气的密度是1.293,NH3的密度是0.771,很明显,标准状况下气体NH3的密度比空气小;
(3)该装置收集密度比空气密度大的长进短出,若用该装置采用排水法收集气体则短进长出排出装置中的水;
故答案是:(1)氧气;(2)小;(3)b.
点评 应熟悉常用的气体收集方法,排空气法要根据气体的密度来确定,但排空气法收集的气体不是很纯;气体用排水法收集的较纯.

练习册系列答案
相关题目
20. 蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:
蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:
①燃烧的产物可能有CO2.
②燃烧的产物可能有H2O.
除了上述猜想,你的猜想,燃烧的产物可能有C或CO或含有C、CO2、H2O和CO四种物质的任意组合.
实验一:在密闭容器中点燃蜡烛至熄灭,抽取10毫升密闭容器中的气体,注入到试管中的饱和澄清石灰水中,发现石灰水始终没有变浑浊,从实验的科学性考虑,下一步是B(选填字母).
A.直接得到燃烧产物中没有CO2的结论
B.再多抽取一些气体注入到试管中的石灰水中
C.增加饱和澄清石灰水的质量
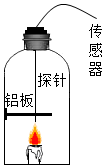
实验二:在老师的指导下,利用多功能传感器进行有关量的测量,装置如图所示,实验结束后,铝板表面有黑色
固体颗粒,同时传感器采得实验前后的有关数据如表所示:
由实验及结果分析,密闭容器内蜡烛熄灭的原因是氧气含量下降,二氧化碳含量上升;蜡烛燃烧生成的产物是C、CO2、H2O和CO.
 蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:
蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:①燃烧的产物可能有CO2.
②燃烧的产物可能有H2O.
除了上述猜想,你的猜想,燃烧的产物可能有C或CO或含有C、CO2、H2O和CO四种物质的任意组合.
实验一:在密闭容器中点燃蜡烛至熄灭,抽取10毫升密闭容器中的气体,注入到试管中的饱和澄清石灰水中,发现石灰水始终没有变浑浊,从实验的科学性考虑,下一步是B(选填字母).
A.直接得到燃烧产物中没有CO2的结论
B.再多抽取一些气体注入到试管中的石灰水中
C.增加饱和澄清石灰水的质量
实验二:在老师的指导下,利用多功能传感器进行有关量的测量,装置如图所示,实验结束后,铝板表面有黑色
固体颗粒,同时传感器采得实验前后的有关数据如表所示:
| 相对湿度 | 氧气含量 | 二氧化碳含量 | 一氧化碳含量 | |
| 蜡烛点燃前 | 48.4% | 18.7% | 0.058% | 0 |
| 蜡烛熄灭后 | 71.6% | 15.6% | 3.643% | 0.0182% |
17.下列物质属于纯净物的是( )
| A. | 冰和水混合物 | B. | 酒精溶液 | C. | 冰冻矿泉水 | D. | 纯净的空气 |
4. 俗话说“人以群分、物以类聚”,化学药品柜也一样,同类别的药品放在同一个柜子里
俗话说“人以群分、物以类聚”,化学药品柜也一样,同类别的药品放在同一个柜子里
(1)马虎在整理药品时,不小心把一位“居民”放错在五号柜里,它是Na2CO3.
(2)六号柜有一位“制氧博士”,实验室由它制取氧气的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)三号柜里住着一位“灭火能手”,检验它的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
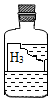
(4)如图是某个同学做实验时从上面的药品柜中取下试剂,因为操作不当标签被部分腐蚀,根据残缺的标签它最适合的位置应该是四号柜.
 俗话说“人以群分、物以类聚”,化学药品柜也一样,同类别的药品放在同一个柜子里
俗话说“人以群分、物以类聚”,化学药品柜也一样,同类别的药品放在同一个柜子里| 药品柜 | 一号柜 | Cu Mg Fe |
| 二号柜 | C P S | |
| 三号柜 | CO2 MgO CuO | |
| 四号柜 | H2SO4 HNO3 HCl | |
| 五号柜 | NaOH Ca(OH)2 Na2CO3 | |
| 六号柜 | KMnO4 NaCl CuSO4 |
(2)六号柜有一位“制氧博士”,实验室由它制取氧气的化学方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)三号柜里住着一位“灭火能手”,检验它的化学方程式:Ca(OH)2+CO2=CaCO3↓+H2O.
(4)如图是某个同学做实验时从上面的药品柜中取下试剂,因为操作不当标签被部分腐蚀,根据残缺的标签它最适合的位置应该是四号柜.
1.为确定某大理石样品的纯度,某兴趣小组进行如下实验:称取该大理石(主要成分是CaCO3;,杂质不参加反应)加入烧杯中,向其中逐渐加入稀盐酸至完全反应.反应结束后,称量烧杯的总质量(溶解的气体忽略不计),有关数据记录如下表.
(1)实验中判断碳酸钙已经完全反应的方法是继续滴入稀盐酸,观察到不再生成气泡.
(2)实验中产生的二氧化碳质量为3.3克,请计算该大理石样品的纯度.(计算结果精确到0.1%)
(3)大理石是重要的建筑材料,在实际应用中应避免与酸性物质(或者酸)接触.
| 烧杯 | 大理石 | 稀盐酸 | 反应后烧杯总质量 | |
| 质量(克) | 90 | 8.5 | 50 | 145.2 |
(2)实验中产生的二氧化碳质量为3.3克,请计算该大理石样品的纯度.(计算结果精确到0.1%)
(3)大理石是重要的建筑材料,在实际应用中应避免与酸性物质(或者酸)接触.
19. 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法不正确的是( )| A. | 将丙物质饱和溶液变为不饱和溶液,可采用降温方法 | |
| B. | 70℃时,分别用100g水配制甲、乙的饱和溶液,再降温到20℃,析出无水晶体的质量:甲>乙 | |
| C. | 50℃时,将等质量的甲、乙、丙三种固体分别配制成饱和溶液,需加水质量最多的是丙 | |
| D. | 将40℃时甲、乙、丙的饱和溶液分别升温至60℃,所得溶液的溶质质量分数由大到小的顺序是:乙>甲=丙 |
