题目内容
10.结合图示实验装置,回答下列问题.
(1)图1中a、b仪器的名称:a锥形瓶,b集气瓶.
(2)如果选用高锰酸钾来制取和收集比较纯净的氧气,应选用的装置是A和D(填字母代号),发生的化学反应方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,棉花团的作用是防止加热时高锰酸钾粉末进入导管.用D装置收集气体是,当集气瓶口有大气泡冒出时,说明集气瓶已收满气体.
(3)若用B装置来制取气体,要控制反应的速率,应将长颈漏斗改为分液漏斗(或注射器);A、B两个制取装置,在装入药品前都应先检查装置的气密性.
(4)实验室制取氢气时,如用E装置收集H2,则气体应从d端通入(填“c”或“d”).用装置C制取氢气,在反应过程中,要停止该反应的操作是关闭活塞,过一会儿反应就会停止,其原因是关闭活塞,试管内的气体无法排出,导致试管内气压增大,将液体压入长颈漏,固液分离,反应停止.
(5)用C装置在实验室制取CO2时,若多孔隔板改成隔离铜网,同样可以制取,若改用隔离铝丝网做,那么产生的后果是收集的二氧化碳不纯,其原因是:2Al+6HCl=2AlCl3+3H2↑(用化学方程式表示),说明金属活动性Cu<Al(选填“>”“<”或“=”).
分析 (1)要掌握各种仪器的名称;
(2)用高锰酸钾固体制氧气需要加热,属于固体加热型,故选发生装置A,收集纯净的氧气用排水法,据反应原理书写方程式,并据注意事项和排水法收集气体分析解答;
(3)要控制反应速率,可将长颈漏斗换为分液漏斗或注射器,装入药品前应该检验气密性;
(4)根据所要收集的气体的密度确定进入的导管,并据密闭装置内压强增大,使固液反应物分离解答.
(5)据铝和盐酸反应生成氢气、铜与盐酸不反应的角度分析.
解答 解:(1)根据图中仪器的图形和用途,a是锥形瓶,b是集气瓶.
(2)用高锰酸钾固体制氧气需要加热,属于固体加热型,故选发生装置A,氧气不易溶于水,所以收集纯净的氧气用排水法,加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应的化学反应方程式2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.加热时试管口放棉花是为了防止加热时高锰酸钾粉末进入导管,利用排水法收集气体时,当集气瓶口有大气泡冒出时则说明收集满了;
(3)若用B装置来制取气体,要控制反应的速率,应将长颈漏斗改为 分液漏斗,分液漏斗下端有一个活塞,可随时控制加入液体的量,或换为注射器;制取气体的装置,在装入药品前都应先 检查装置的气密性,防止装置漏气;
(4)实验室制取氢气时,如用E装置收集H2,由于氢气的密度比空气小,则气体应从 d端通入,将空气挤压到集气瓶底部从c端排出;用装置C制取氢气,在反应过程中,将导管处的活塞关闭,则试管内产生H2不能导出,气体压强增大,导致试管内液面下降,使液体与固体脱离接触,反应将自行停止;
(5)用C装置在实验室制取CO2时,若多孔隔板改成隔离铜网,同样可以制取,因为铜与盐酸不反应,如改用隔离铝丝网,那么产生的后果是 收集的气体不纯,其原因是铝的化学性质比较活泼,能和盐酸反应生成氢气,反应的化学方程式 是:2Al+6HCl=2AlCl3+3H2↑;铜与盐酸不反应,说明铜排在顺序表中氢的后面,铝与盐酸反应说明铝排在顺序表中氢的前面,则铝的活动性比铜强;
故答案为:
(1)锥形瓶;集气瓶;
(2)A;D;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;防止加热时高锰酸钾粉末进入导管;集气瓶口有大气泡冒出;
(3)分液漏斗(或注射器);检查装置的气密性.
(4)d;关闭活塞,试管内的气体无法排出,导致试管内气压增大,将液体压入长颈漏,固液分离,反应停止;
(5)收集的二氧化碳不纯;2Al+6HCl=2AlCl3+3H2↑;<.
点评 本题主要考查气体的制取方法和化学方程式的书写、实验注意事项等方面的知识,书写化学方程式时要注意遵循质量守恒定律,所以同学们要加强基础知识的积累,以便灵活运用.

 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案| A. | 在水净化的单一操作中,蒸馏是净化程度较高的方法之一 | |
| B. | 常用肥皂水检验硬水和软水 | |
| C. | 为节约用水,农业、园林浇灌改大水漫灌为喷灌、滴灌 | |
| D. | 海洋有自净能力,所以不存在海水污染问题 |
| A. | 属于氧化物 | |
| B. | 它是由两个碳原子、六个氢原子和一个氧原子构成的 | |
| C. | 碳、氢、氧元素的质量比为2:6:1 | |
| D. | 它是由碳、氢、氧三种元素组成的 |
(1)提出假设:气体产物全部是CO2.

(2)查阅资料:a.氮气不能与炭粉及Fe2O3反应.
b.高温下可以发生下列反应:2Fe2O3+3C$\frac{\underline{\;高温\;}}{\;}$4Fe+3CO2↑ C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO
(3)设计方案:将一定量氧化铁在隔绝空气的环境下与过量炭粉充分反应.用实验中实际测得产生气体的质量,与理论计算得到的CO2的质量进行比较.
(4)实验装置:如图所示.
(5)实验操作:
①称量:反应前Fe2O3的质量3.20g;炭粉的质量2.00g;玻璃管C的质量48.48g.反应后玻璃管与残留固体共52.24g.
②加热前先通一段时间氮气,再夹紧弹簧夹T,点燃酒精喷灯加热.
(6)问题分析:①用酒精喷灯而不用酒精灯的目的是获取反应所需的高温条件.
②加热前先通一段时间氮气的目的是清除试管中空气(氧气),防止炭粉与空气中氧气发生反应.
③理论计算:若氧化铁与炭粉反应的气体产物全部是CO2,求3.20g氧化铁完全反应时生成CO2的质量.(写出计算过程)
④根据实验数据计算实验中实际获得气体的质量.(写出计算过程)
(7)结论:原假设不能(能、不能)成立,理由是因为生成的气体质量为1.44 g,大于1.32 g,故气体产物不完全为CO2,实际是C02和C0的混合物,原假设不能成立(其他合理答案亦可给分).
(8)兴趣小组成员小聪想到家里新换的水龙头.他从说明书上了解到该水龙头是铜质镀铬.好奇的小聪想探究铬(Cr)与常见金属铁、铜的活动性强弱,请你参与.
【作出猜想】
猜想1:Cr>Fe>Cu; 猜想2:Fe>Cu>Cr; 猜想3:你的猜想是Fe>Cr>Cu.
【查阅资料】
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜.
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液.
【设计与实验】
小聪同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸.
| 实验 | 试管1 | 试管2 | 试管3 |
| 实验 操作 |  |  |  |
| 实验 现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | 铜表面无气泡 |
①小聪得到的结论是猜想1正确.
②实验前用砂纸打磨金属片的目的是除去金属表面的氧化膜,利于反应.
【知识运用】
将铬片投入FeSO4溶液中,反应能(填“能”或“不能”)进行.若能进行,请你写出化学方程式Cr+FeSO4=Fe+CrSO4.
| A. | 自来水 | B. | 汽水 | C. | 蒸馏水 | D. | 盐水 |

 如图是验证分子性质的装置.U型管左侧管内固定一小试管,右侧管内挂有滴有酚酞溶液的滤纸条,胶头滴管中有浓氨水.
如图是验证分子性质的装置.U型管左侧管内固定一小试管,右侧管内挂有滴有酚酞溶液的滤纸条,胶头滴管中有浓氨水.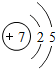 氮原子最外层电子数为5.
氮原子最外层电子数为5.