题目内容
18.氧是地壳中含量最多的元素,有两种氧原子可以分别表示为为${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O,左下角数字表示质子数,左上角数字表示质子数和中子数之和,则( )| A. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 互为同位素原子 | |
| B. | ${\;}_{8}^{18}$O 的核外电子数多于${\;}_{8}^{16}$O | |
| C. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 属于同种原子 | |
| D. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 的核内中子数相等 |
分析 A、根据同位素的概念判断.
B、根据核外电子数等于核内质子数判断;
C、根据同种原子是指质子数、中子数、电子数都相等进行解答;
D、根据题目所给符号,可知二者的中子是分别为8和10进行解答;
解答 解:A、质子数相同而中子数不同的同一元素的不同原子互称为同位素,即二者质子数都是8,中子数分别为10和8.故A说法正确;
B、核外电子数等于核内质子数,因二者的质子数相等,故核外电子数也相等,故B错误;
C、二者属于同种元素,但不是同种原子,故C错误;
D、二者核内的中子数分别为10和8,故D错误;
故选A.
点评 本题考查的是常用的基本概念和基本理论,属于识记和理解的范畴,需要认真总结和反复应用.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
6. 为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
(1)请完成证明金属粉末中存在Fe和Cu的实验设计:
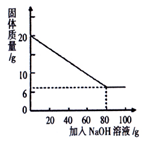
(2)为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,则该金属粉末中Al的质量分数为70%.
 为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.
为证明由三种金属组成的混合粉末中,Fe和Cu的存在并测定其中Al的质量分数,某科学兴趣小组的同学展开了下列的实验探究.查阅资料得:Al与氢氧化钠溶液反应生成溶于水的偏铝酸钠和氢气(反应的化学方程式为:2Al+2H2O+2NaOH=2NaAlO2+3H2↑),Fe和Cu不与氢氧化钠溶液反应.| 实验操作 | 实验现象 | 结论 |
| I.取少量的金属粉末于试管中,加入足量的氢氧化钠溶液 | 有气泡产生 | 仅除去铝 |
| II.将试管静置,弃去上层清液,加入足量的稀盐酸 | 有气泡产生 | 证明含有铁 |
| III.将试管静置,弃去上层清液,多次洗涤剩余固体 | 剩余固体 呈紫红色 | 证明含有铜 |
(2)为探究该金属粉末中Al的质量分数,取20g该金属粉末,加入氢氧化钠溶液反应,剩余固体质量与所加氢氧化钠溶液的质量关系如图所示,则该金属粉末中Al的质量分数为70%.
13.一瓶未贴标签的粉末状常见金属R.为测定R的相对原子质量,准确称取一定量该金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重.重复实验,获得如表数据.请回答:
(1)表格中m=85.0.
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取0.6克氢气,至少需要质量分数为10%的稀硫酸溶液多少克?
| 实验次数 | 金属质量(g) | 金属氧化物质量(g) |
| l | 45.0 | 84.9 |
| 2 | 45.0 | 85.1 |
| 3 | 45.0 | 85.0 |
| 平均值 | 45.0 | m |
(2)已知R的化合价为+3价,则R的相对原子质量为27.
(3)若用该金属与稀硫酸反应制取0.6克氢气,至少需要质量分数为10%的稀硫酸溶液多少克?
3.育华学校初二科学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)有关实验数据如下表:
(1)根据质量守恒定律可知,反应中生成二氧化碳的质量为4.4g.
(2)反应中生成氯化钙多少克?
(3)该石灰石中碳酸钙的质量分数为多少?
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150 g | 12 g | 157.6 g | |
(2)反应中生成氯化钙多少克?
(3)该石灰石中碳酸钙的质量分数为多少?
7.某工厂排放的废气中CO2、SO2均超标,技术人员采用下列哪种方法治理废气是正确的( )
| A. | 用NaCl溶液吸收 | B. | 用NaOH 溶液吸收 | ||
| C. | 用浓HCl溶液吸收 | D. | 用浓H2SO4溶液吸收 |
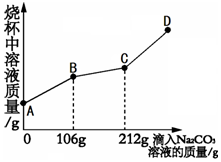 在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题:
在一烧杯中盛有l00克BaCl2和HCl的混合溶液,向其中逐渐滴加溶质质量分数为10%的Na2CO3溶液,混合溶液的质量与所滴入Na2CO3溶液的质量关系曲线如图所示,请根据题意问答问题: