题目内容
3.育华学校初二科学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水,杂质中不含钙元素)有关实验数据如下表:| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 150 g | 12 g | 157.6 g | |
(2)反应中生成氯化钙多少克?
(3)该石灰石中碳酸钙的质量分数为多少?
分析 (1)根据质量守恒定律,在化学反应中,参加反应前各物质的质量总和等于反应后生成各物质的质量总和.反应生成二氧化碳的质量=参加反应前各物质的质量总和-反应后生成各物质的质量总和进行分析;
(2)根据碳酸钙与盐酸反应的化学方程式和生成二氧化碳的质量,可以计算生成氯化钙的质量进行分析;
(3)根据化学方程式和二氧化碳的质量可以计算石灰石中碳酸钙的质量分数进行分析.
解答 解:(1)由质量守恒定律可知,生成二氧化碳的质量为:150g+12g-157.6g=4.4g;
(2)设生成氯化钙x,该石灰石样品中碳酸钙的质量为y,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100 111 44
y x 4.4 g
$\frac{100}{y}$=$\frac{111}{x}$=$\frac{44}{4.4g}$
x=11.1g
y=10g
(3)该石灰石中碳酸钙的质量分数为:$\frac{10g}{12g}$×100%=83.3%.
故答案为:(1)4.4;
(2)11.1;
(3)83.3%.
点评 本题主要考查学生运用质量守恒定律、化学方程式和质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 能考试期末冲刺卷系列答案
能考试期末冲刺卷系列答案
相关题目
14.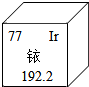 2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.如图所示是元素周期表中的一格,有关说法错误的是( )
2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.如图所示是元素周期表中的一格,有关说法错误的是( )
 2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.如图所示是元素周期表中的一格,有关说法错误的是( )
2014年5月7日在南京丢失的放射源铱-192,于5月10日安全回收.铱-192是高危放射源,会危害人体健康.如图所示是元素周期表中的一格,有关说法错误的是( )| A. | 铱元素是金属元素 | |
| B. | 铱-192原子的质子数为77,中子数为115 | |
| C. | 铱元素的相对原子质量为192.2g | |
| D. | 铱-192和铱-191、铱-193属于同位素原子 |
18.氧是地壳中含量最多的元素,有两种氧原子可以分别表示为为${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O,左下角数字表示质子数,左上角数字表示质子数和中子数之和,则( )
| A. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 互为同位素原子 | |
| B. | ${\;}_{8}^{18}$O 的核外电子数多于${\;}_{8}^{16}$O | |
| C. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 属于同种原子 | |
| D. | ${\;}_{8}^{18}$O 和${\;}_{8}^{16}$O 的核内中子数相等 |
 利用如图测定空气中氧气的含量,你所看到的现象:红色变成黑色,实验测得空气中氧气的含量为19.2%,请分析该实验出现的误差的原因是注射器的活塞摩擦力较大;注射器的分度值较大(举例一种)
利用如图测定空气中氧气的含量,你所看到的现象:红色变成黑色,实验测得空气中氧气的含量为19.2%,请分析该实验出现的误差的原因是注射器的活塞摩擦力较大;注射器的分度值较大(举例一种)


