题目内容
7.工业生产中,多数金属的冶炼过程都是采用热还原法.为测定某样品中三氧化钨的质量分数,我校化学课外活动小组的同学根据此原理,采用如图所示装置进行实验.
样品的质量为13.0g,化学方程式为WO3+3H2$\frac{\underline{\;高温\;}}{\;}$W+3H2O,样品中的杂质不参加反,WO3完全反应,C中吸收完全.小组同学经过规范的实验操作后得到了两组数据,记录如表所示.对于该实验,有以下几种说法:
| 实验 | 装置的质量 | 实验前 | 实验后 |
| 第一组 | B装置的 总质量/g | 45.5 | 43.1 |
| 第二组 | C装置的 总质量/g | 100.5 | 103.3 |
②实验前应先向装置中通入氢气,防止加热时产生爆炸;
③反应前后装置B减少的质量为生成水的质量;
④该实验没有尾气处理装置,容易造成空气污染;
⑤利用实验前后装置B的总质量进行计算,得到的结果更准确;
⑥若B中的WO3没有完全反应,对测定结果没有影响
以上说法中,正确的是( )
| A. | ①②③ | B. | ③④⑤ | C. | ③④⑥ | D. | ①②⑤ |
分析 根据实验过程中所发生的化学反应、氢气没有干燥、装置B中玻璃管减少的质量以及装置C增重的质量来分析解答.
解答 解:①锌与稀硫酸反应生成硫酸锌和氢气、WO3+3H2$\frac{\underline{\;高温\;}}{\;}$W+3H2O,二者均属于一种单质与一种化合物反应生成另一种单质与另一种化合物,属于置换反应,故正确;
②氢气具有可燃性,所以在加热前,要先向将装置内通入氢气,为了排净装置内的空气,以免加热时发生爆炸,故正确;
③反应前后装置B减少的质量为生成的水中氧元素的质量,故错误;
④尾气中主要是氢气,氢气无毒,不会造成空气的污染,故错误;
⑤因为氢气没有干燥,所以若用装置C增重的质量来计算样品的纯度不准确,所以利用实验前后装置B的总质量进行计算,得到的结果更准确,故正确;
⑥测定某样品中三氧化钨的质量分数,B中的WO3必须完全反应,故错误.
故选D.
点评 本题中,判断以哪组数据为标准可能会出错,一定注意C装置也可以吸收空气中的水蒸气.

练习册系列答案
 导学全程练创优训练系列答案
导学全程练创优训练系列答案
相关题目
18.下列实验方案的设计中,没有正确体现对比思想的是( )
| A. | 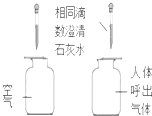 比较二氧化碳的含量 | |
| B. | 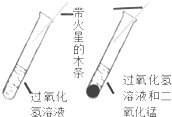 研究二氧化锰的催化作用 | |
| C. |  区分硬水和软水 | |
| D. | 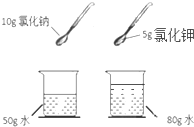 常温下比较氯化钠和氯化钾的溶解能力 |
15.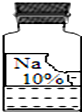 实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)
实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)
小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ.室温(20℃)时,测定四种物质的溶解度数据如表:
小华根据试剂瓶标注的质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是NaHCO3 .
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是NaOH.
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是NaCl溶液.
(2)小强为了检验该溶液是剩余两个猜想中的哪一个,他又进行了如表实验.
 实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)
实验室里有一瓶常用的无色溶液,因保管不当,其残缺的标签中只剩下“Na”和“10%”字样(如图所示)小强和小华同学很感兴趣,决定对其成分进行探究.
【提出问题】这瓶试剂可能是什么溶液呢?
【交流讨论】根据受损标签的情况判断,这瓶试剂不可能是A
A.酸 B.碱 C.盐
【查阅资料】
Ⅰ.初中常见含钠的化合物有:NaCl、NaOH、Na2CO3、NaHCO3.
Ⅱ.Na2CO3和NaHCO3的水溶液都呈碱性.
Ⅲ.室温(20℃)时,测定四种物质的溶解度数据如表:
| 物 质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度/g | 36 | 109 | 215 | 9.6 |
【作出猜想】①可能是NaCl;②可能是Na2CO3;③可能是NaOH.
【实验探究】
(1)小强用洁净的玻璃棒蘸取试液于pH试纸上,测得pH>7,则这瓶试剂不可能是NaCl溶液.
(2)小强为了检验该溶液是剩余两个猜想中的哪一个,他又进行了如表实验.
| 实验步骤 | 实验现象 | 结论及化学方程式 |
| 取少量溶液于试管中,滴加BaCl2溶液. | 产生白色沉淀 | 猜想②正确. 反应的化学方程式:BaCl2+Na2CO3=BaCO3+NaCl. |
2.下列四个图象中,能正确反映其对应变化关系的是( )
| A. |  分别用等质量、等质量分数的过氧化氢溶液制取氧气 | |
| B. |  向一定量的稀盐酸中加入足量的水稀释 | |
| C. |  向等质量、等质量分数的稀盐酸中分别逐渐加入锌粉、镁粉至过量 | |
| D. |  在密闭容器中通电分解水 |
12.下列图象分别与选项中的操作相对应,其中合理的是( )


| A. | 向氢氧化钠和硝酸钡的混合溶液中加入足量的稀硫酸 | |
| B. | 向一定量氯化铜溶液中加入铝 | |
| C. | 红磷在装有空气的密闭容器中燃烧 | |
| D. | 向等质量、等质量分数的稀硫酸中分别加入锌粉和铁粉 |
 如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质的溶解度曲线,a与c的溶解度曲线相交于P点.据图回答: 小明在元素周期表中查找到如图所示的一格后,明白了不能把一氧化碳写成“Co”的原因.
小明在元素周期表中查找到如图所示的一格后,明白了不能把一氧化碳写成“Co”的原因.