题目内容
6.实验室常用下列装置来制取气体:
(1)写出如图1中有标号仪器的名称:a锥形瓶.
(2)用实验室用氯酸钾制取氧气时,发生反应的化学方程式为2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑.发生装置选A.
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下NH3是一种无色、有刺激性气味的气体,密度比空气小,NH3极易溶于水,若用F装置来收集NH3,气体应从N导管口进入.(选填“M”或“N”)
(4)小明用大理石与稀盐酸反应制取CO2,可选用的装置组合是BE.方程式为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(5)如图2是小明实验时的主要步骤,这些步骤的正确顺序是(填字母标号,下同)cabde,其中操作有误的是d.
分析 锥形瓶是常用的反应容器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.若用F装置来收集NH3,气体应从短管进入,因为氨气的密度比空气小;如图2是小明实验时的主要步骤,这些步骤的正确顺序是cabde,其中操作有误的是验满,验满时,燃着的木条应该放在集气瓶口.
解答 解:(1)锥形瓶是常用的反应容器,故答案为:锥形瓶;
(2)如果用氯酸钾制氧气就需要加热,氯酸钾在二氧化锰做催化剂和加热的条件下生成氯化钾和氧气,配平即可;故答案为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;A;
(3)若用F装置来收集NH3,气体应从短管进入,因为氨气的密度比空气小;故答案为:N;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;故答案为:BE;CaCO3+2HCl=CaCl2+H2O+CO2↑;
(5)如图2是小明实验时的主要步骤,这些步骤的正确顺序是cabde,其中操作有误的是验满,验满时,燃着的木条应该放在集气瓶口;故答案为:cabde;d;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 阅读快车系列答案
阅读快车系列答案| A. | Na+、NO3-、Ba2+ | B. | Cu2+、OH-、SO42- | C. | Cu2+、Mg2+、SO42- | D. | Ba2+、NO3-、Mg2+ |
| A. |  干冰升华 | B. |  CO2溶于水 | ||
| C. | 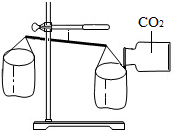 实验CO2的密度 | D. |  自制过滤器过滤液体 |
| A. | 不纯的氢气燃烧发生爆炸 | B. | 涂在墙上的熟石灰逐渐变硬 | ||
| C. | 焦炭冶炼金属 | D. | 舞台上用干冰制造“云雾” |
| A. | CO2溶解在水中形成碳酸 | B. | 水4℃时密度最大,为1g/cm3 | ||
| C. | 水不能燃烧 | D. | 水通电产生氢气和氧气 |

 如图是电解水的简易装置.
如图是电解水的简易装置. 实验室过滤器如图所示.
实验室过滤器如图所示.