题目内容
15. 实验室制取气体时,首先要选择反应物,明确如何控制反应条件,然后确定气体发生和收集装置,还要考虑装置是否符合环保、安全等要求.请回答以下问题:
实验室制取气体时,首先要选择反应物,明确如何控制反应条件,然后确定气体发生和收集装置,还要考虑装置是否符合环保、安全等要求.请回答以下问题:(1)实验室制取氧气时,下列物质不能直接作为制氧原料的是②④(填序号),判断的依据是组成中是否含有氧元素.
①水 ②氯化钠 ③高锰酸钾(MnO4) ④甲烷(CH4) ⑤过氧化氢
(2)当确定了实验室制取某种气体的化学反应原理后,还应该考虑原料是否容易获得、实验条件是否易于控制或操作是否简便或实验操作是否安全可靠等等因素(写一项即可).选择气体的收集方法时,以下气体性质中需要考虑的因素是②④(填序号).
①颜色 ②密度 ③可燃性 ④溶解性
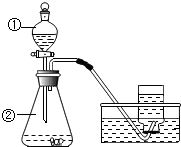
(3)如图所示是实验室制取氧气的实验装置,指出图中有标号仪器的名称:①分液漏斗,②锥形瓶;用双氧水制取氧气的化学反应方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;.用图中方法收集氧气的原因是氧气不易溶于水;当导管口的气泡连续、均匀冒出时,开始收集;收集满时看到的现象是瓶口有大气泡冒出.
(4)用图中的气体发生装置还可以制取的气体是二氧化碳,收集该气体应采用的方法是向上排空气法;检验这种气体收集满集气瓶的方法是将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;制取该气体反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.
分析 分液漏斗方便加液体药品,锥形瓶是常用的反应仪器,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了.当确定了实验室制取某种气体的化学反应原理后,还应该考虑原料是否容易获得、实验条件是否易于控制或操作是否简便或实验操作是否安全可靠等;气体的收集装置的选择与气体的密度和溶解性有关.
解答 解:(1)实验室制取氧气时,不能直接作为制氧原料的是:氯化钠和甲烷;判断的依据是:组成中是否含有氧元素;故答案为:②④;组成中是否含有氧元素;
(2)当确定了实验室制取某种气体的化学反应原理后,还应该考虑原料是否容易获得、实验条件是否易于控制或操作是否简便或实验操作是否安全可靠等;气体的收集装置的选择与气体的密度和溶解性有关;故答案为:实验条件是否易于控制或操作是否简便或实验操作是否安全可靠等;②④;
(3)分液漏斗方便加液体药品,锥形瓶是常用的反应仪器,如果用双氧水和二氧化锰制氧气就不需要加热,氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;收集满时看到的现象是:瓶口有大气泡冒出;故答案为:分液漏斗;锥形瓶;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;氧气不易溶于水;连续、均匀;瓶口有大气泡冒出;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集;二氧化碳的验满方法是:将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;故答案为:二氧化碳;向上排空气法;将一根燃着的木条平放在集气瓶口,木条熄灭,证明满了;CaCO3+2HCl=CaCl2+H2O+CO2↑;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的验满等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 优加精卷系列答案
优加精卷系列答案| A. |  将足量碳酸镁和氧化镁固体分别加入相同质量、相同质量分数的稀盐酸中 | |
| B. |  在一定温度下,向不饱和的硝酸钠溶液中不断加入硝酸钠固体,充分搅拌 | |
| C. |  向一定量的氯化钠溶液中滴加稀硫酸至过量 | |
| D. |  向一定量的硫酸和硫酸镁混合溶液中滴加氢氧化钡溶液 |
 人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝.结合图中信息判断,下列叙述正确的是( )
人体缺碘会引起甲状腺肿大,幼儿缺碘影响生长发育,造成思维迟钝.结合图中信息判断,下列叙述正确的是( )| A. | 碘的相对原子质量是126.9g | |
| B. | 碘属于金属元素 | |
| C. | 碘的核电荷数是53 | |
| D. | 碘原子核外有5个电子层,参加化学反应时易失去最外层电子 |
| A. |  易失电子 | B. |  易形成阴离子 | C. |  阳离子 | D. |  化学性质稳定 |
①氧化 ②融化 ③升华 ④催化.
| A. | ①② | B. | ①③ | C. | ①④ | D. | ②③ |

| A. | 20℃时,100g甲溶液中含甲物质的质量为25g | |
| B. | 20℃时,甲、乙饱和溶液中含溶质的质量相等 | |
| C. | 30℃时,甲、乙两物质的饱和溶液中溶质的质量分数甲大于乙 | |
| D. | 50℃时,将甲、乙两种物质的饱和溶液分别降温至20℃析出晶体的质量甲大于乙 |


