题目内容
6.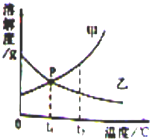 如图是甲、乙两种物质的溶解度曲线,看图回答下列问题:
如图是甲、乙两种物质的溶解度曲线,看图回答下列问题:(1)P点的含义是t1℃时甲、乙两物质的溶解度相等.
(2)青海盐湖地区有一种说法,“冬天捞碱,夏天晒盐”.其中“碱”的溶解度曲线与图中甲(填“甲”或“乙”)物质的溶解度曲线相似.
(3)欲使接近饱和的乙溶液变成饱和溶液,可以采取的方法是升高温度(答一种即可).
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)P点的含义是:t1℃时甲、乙两物质的溶解度相等;
(2)冬天捞碱,夏天晒盐,说明降低温度碱的溶解度变小,所以碱”的溶解度曲线与图中甲物质的溶解度曲线相似;
(3)乙物质的溶解度随温度的升高而减小,所以欲使接近饱和的乙溶液变成饱和溶液,可以采取的方法是升高温度.
故答案为:(1)t1℃时甲、乙两物质的溶解度相等;
(2)甲;
(3)升高温度.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
14.下列化合物中,氮元素的化合价由低到高排列的是( )
| A. | NO NO2 NH3 HNO3 | B. | NO NH3NO2HNO3 | ||
| C. | NH3 NO NO2 HNO3 | D. | HNO3NO2NH3NO |
11.下表是Ca(OH)2和NaOH的溶解度数据.请回答下列问题:
(1)依据上表数据,绘制Ca(OH)2和NaOH的溶解度曲线,图中能表示NaOH溶解度曲线的是A(填A或B).

(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②降低温度,③升高温度,④加入水,⑤加入生石灰,⑥蒸发水后再恢复到原温度.其中措施正确的是①③⑤⑥(填序号).
(3)60℃时,229g 饱和NaOH溶液,加热蒸发50g水后,再降温到20℃,可析出NaOH固体的质量为83.5g.
(4)现有80℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH固体,应采取的物理方法是降温结晶,过滤.
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 | |
| 溶解度/g | Ca(OH)2 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 | 0.08 |
| NaOH | 31 | 91 | 111 | 129 | 313 | 336 | |

(2)要想把一瓶接近饱和的Ca(OH)2溶液变成饱和溶液,具体措施有:
①加入氢氧化钙,②降低温度,③升高温度,④加入水,⑤加入生石灰,⑥蒸发水后再恢复到原温度.其中措施正确的是①③⑤⑥(填序号).
(3)60℃时,229g 饱和NaOH溶液,加热蒸发50g水后,再降温到20℃,可析出NaOH固体的质量为83.5g.
(4)现有80℃时含Ca(OH)2和NaOH两种溶质的饱和溶液,若要得到较纯净的NaOH固体,应采取的物理方法是降温结晶,过滤.
18.下列物质在空气中久置后其水分明显增加的是( )
| A. | 浓HCl | B. | 浓H2SO4 | C. | 浓HNO3 | D. | 食盐水 |
15.如图所示变化属于化学变化的是( )
| A. |  对玻璃片呼气 | B. |  蜡烛燃烧 | C. |  灯泡通电发光 | D. |  湿衣晾干 |
16.某集气瓶中盛有氮气和氧气的混合气体(体积比为4:1),采用燃烧法除去氧气而得到较纯净的氮气时,最好采用的物质是( )
| A. | 铁丝 | B. | 红磷 | C. | 木炭 | D. | 硫磺 |