题目内容
18.已知在水溶液中,乙醇(C2H5OH)不发生电离,溴化氢(HBr)电离产生氢离子(H+)和溴离子(Br-),氢氧化钠电离产生钠离子和氢氧根离子.请回答下列问题:(1)根据这三种溶液的组成推断,医用酒精(含乙醇75%的水溶液)显中性(填“酸性”、“中性”或“碱性”);
(2)写出上述物质之间发生中和反应的化学方程式HBr+NaOH═NaBr+H2O;
(3)氢氧化钠溶液中存在的微粒有(用化学符号表示)H2O、Na+、OH-.
分析 有的溶液显酸性或碱性是因为这些溶液中含有氢离子或氢氧根离子,只有酸和碱发生的反应才是中和反应.
解答 解:(1)由于酒精在水溶液中不发生电离,在它的溶液中也就没有氢离子或者是氢氧根离子,所以酒精溶液既不显酸性也不显碱性;
故答案为:中性;
(2)由于溴化氢电离时生成的阳离子只有氢离子,说明它是酸,而氢氧化钠是碱,故它们发生的反应是中和反应;
故答案为:HBr+NaOH═NaBr+H2O;
(3)氢氧化钠溶液是氢氧化钠的水溶液;
故答案为:H2O、Na+、OH-.
点评 本题难度不是很大,主要考查了有关酸的化学性质及中和反应的应用,培养学生的理解能力和分析能力.

练习册系列答案
相关题目
9.比较如图两种粒子的结构示意图得到的下列说法中,正确的是( )
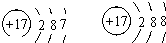
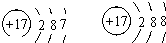
| A. | 二者属于同一种粒子 | B. | 二者属于同一种元素 | ||
| C. | 两粒子的化学性质相同 | D. | 都是稳定结构 |
5.某研究小组对用H2O2分解产生H2O和O2 的实验条件进行探究,他们进行了以下实验:①向盛有5mL5%的H2O2溶液的试管中,伸入带火星的木条,木条不复燃.②向盛有5mLA%的H2O2溶液的试管中,加入agMnO2,伸入带火星的木条,木条复燃.③向盛有5mLA%的H2O2溶液的试管中,加入agFe2O3,伸入带火星的木条,木条复燃.④经检验,②、③中反应后试管中仍分别含有agMnO2 和agFe2O3.
(1)实验②、③中H2O2溶液的浓度A%以5%为宜.MnO2 和Fe2O3在上述反应中的作用催化作用,写出③中的反应方程式2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑,该反应属于分解反应.(填反应类型)
(2)研究小组还对溶液的浓度、催化剂的种类等实验条件对反应速率的影响进行了探究.下表选取了部分实验数据:用足量等体积的H2O2溶液制取相同体积的O2所需的时间.
从上表中能得出哪些有关结论?①相同条件下,MnO2的催化效果比Fe2O3好;②在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快.
(1)实验②、③中H2O2溶液的浓度A%以5%为宜.MnO2 和Fe2O3在上述反应中的作用催化作用,写出③中的反应方程式2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑,该反应属于分解反应.(填反应类型)
(2)研究小组还对溶液的浓度、催化剂的种类等实验条件对反应速率的影响进行了探究.下表选取了部分实验数据:用足量等体积的H2O2溶液制取相同体积的O2所需的时间.
| 浓度 时间 条件 | 30%的H2O2溶液 | 15%的H2O2溶液 | 5%的H2O2溶液 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
 如图是化学家研究出的高效、经济的制氢途径.
如图是化学家研究出的高效、经济的制氢途径.
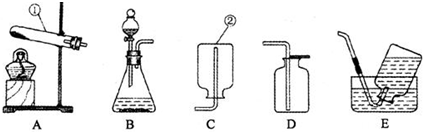
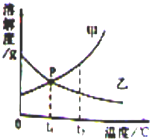 如图是甲、乙两种物质的溶解度曲线,看图回答下列问题:
如图是甲、乙两种物质的溶解度曲线,看图回答下列问题: