题目内容
14.下列化合物中,氮元素的化合价由低到高排列的是( )| A. | NO NO2 NH3 HNO3 | B. | NO NH3NO2HNO3 | ||
| C. | NH3 NO NO2 HNO3 | D. | HNO3NO2NH3NO |
分析 根据在化合物中正负化合价代数和为零,结合各选项中的化学式进行解答本题.
解答 解:氧元素显-2价,设一氧化氮中氮元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-2)=0,则x=+2.
氧元素显-2价,设二氧化氮中氮元素的化合价是y,根据在化合物中正负化合价代数和为零,可得:y+(-2)×2=0,则y=+4.
氢元素显+1价,设氨气中氮元素的化合价是z,根据在化合物中正负化合价代数和为零,可得:z+(+1)×3=0,则z=-3.
氢元素显+1价,氧元素显-2价,设HNO3中氮元素的化合价是m,根据在化合物中正负化合价代数和为零,可得:(+1)+m+(-2)×3=0,则m=+5.
故氮元素化合价由低到高排列的一组是NH3、NO、NO2、HNO3.
故选:C.
点评 本题难度不大,考查学生利用化合价的原则计算指定元素的化合价的能力.

练习册系列答案
相关题目
5.某研究小组对用H2O2分解产生H2O和O2 的实验条件进行探究,他们进行了以下实验:①向盛有5mL5%的H2O2溶液的试管中,伸入带火星的木条,木条不复燃.②向盛有5mLA%的H2O2溶液的试管中,加入agMnO2,伸入带火星的木条,木条复燃.③向盛有5mLA%的H2O2溶液的试管中,加入agFe2O3,伸入带火星的木条,木条复燃.④经检验,②、③中反应后试管中仍分别含有agMnO2 和agFe2O3.
(1)实验②、③中H2O2溶液的浓度A%以5%为宜.MnO2 和Fe2O3在上述反应中的作用催化作用,写出③中的反应方程式2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑,该反应属于分解反应.(填反应类型)
(2)研究小组还对溶液的浓度、催化剂的种类等实验条件对反应速率的影响进行了探究.下表选取了部分实验数据:用足量等体积的H2O2溶液制取相同体积的O2所需的时间.
从上表中能得出哪些有关结论?①相同条件下,MnO2的催化效果比Fe2O3好;②在其他条件相同的情况下,H2O2浓度越大,产生氧气的速度越快.
(1)实验②、③中H2O2溶液的浓度A%以5%为宜.MnO2 和Fe2O3在上述反应中的作用催化作用,写出③中的反应方程式2H2O2$\frac{\underline{\;Fe_{2}O_{3}\;}}{\;}$2H2O+O2↑,该反应属于分解反应.(填反应类型)
(2)研究小组还对溶液的浓度、催化剂的种类等实验条件对反应速率的影响进行了探究.下表选取了部分实验数据:用足量等体积的H2O2溶液制取相同体积的O2所需的时间.
| 浓度 时间 条件 | 30%的H2O2溶液 | 15%的H2O2溶液 | 5%的H2O2溶液 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
9.下列关于二氧化碳的说法错误的是( )
| A. | 二氧化碳可用于制碳酸类饮料 | |
| B. | 二氧化碳可导致温室效应,温室效应对人类有利也有害 | |
| C. | 二氧化碳是不能供给呼吸有毒气体 | |
| D. | 大气中二氧化碳的消耗途径主要是植物的光合作用 |
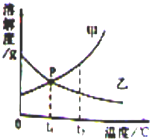 如图是甲、乙两种物质的溶解度曲线,看图回答下列问题:
如图是甲、乙两种物质的溶解度曲线,看图回答下列问题: 某同学做镁条燃烧实验,他夹持镁条应该用的仪器是坩埚钳,在酒精灯火焰上点燃镁条后,他观察到能证明镁条燃烧是化学变化的依据的实验现象是生成白色固体.写出该反应的表达式:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.
某同学做镁条燃烧实验,他夹持镁条应该用的仪器是坩埚钳,在酒精灯火焰上点燃镁条后,他观察到能证明镁条燃烧是化学变化的依据的实验现象是生成白色固体.写出该反应的表达式:2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO.