题目内容
11.以下物质:①金刚石②干冰③石墨④一氧化碳(1)可用于人工降雨的是②(填序号,下同);(2)可用来切割玻璃的是①;(3)具有毒性的气体是④;(4)具有还原性的固体单质是③.
分析 (1)干冰升华时能够吸收热量;
(2)金刚石的硬度很大;
(3)一氧化碳有毒;
(4)石墨是由碳元素组成的单质,具有还原性.
解答 解:(1)干冰能够用来进行人工降雨.故填:②.
(2)金刚石可以用来切割玻璃.故填:①.
(3)一氧化碳是一种有毒的气体.故填:④.
(4)石墨具有还原性.故填:③.
点评 本题主要考查物质的性质和用途,解答时要充分理解各种物质的性质,然后再根据物质的性质方面进行分析、判断,从而确定物质的用途.

练习册系列答案
相关题目
1.下列对应关系不正确的是( )
| A. | 醋、味精--调味品 | |
| B. | 酒精、汽油--易燃液体 | |
| C. | Na+、Fe3+--人体所需微量元素 | |
| D. | 废塑料瓶、铝制易拉罐--可回收垃圾 |
6.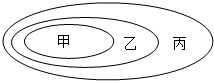 图中甲、乙、丙三个椭圆分别代表某个概念或某类物质.下列能构成图示关系的是( )
图中甲、乙、丙三个椭圆分别代表某个概念或某类物质.下列能构成图示关系的是( )
 图中甲、乙、丙三个椭圆分别代表某个概念或某类物质.下列能构成图示关系的是( )
图中甲、乙、丙三个椭圆分别代表某个概念或某类物质.下列能构成图示关系的是( )| A. | 甲是杠杆、乙是滑轮、丙是简单机械 | |
| B. | 甲是动能、乙是势能、丙是机械能 | |
| C. | 甲是碱、乙是化合物、丙是纯净物 | |
| D. | 甲是化合反应、乙是分解反应、丙是置换反应 |
1. 老师向同学们展示了一瓶标签受损的无色溶液(如图所示),并要求同学们进行探究.
老师向同学们展示了一瓶标签受损的无色溶液(如图所示),并要求同学们进行探究.
【提出问题】这瓶无色溶液是什么溶液?
【提出猜想】老师提示:这瓶无色溶液可能是下列四种溶液中的一种:
①MgSO4 ②Na2SO4 ③H2SO4 ④BaSO4
【查阅资料】:Na2SO4的水溶液显中性.
【实验探究】
(1)依据溶解度性,猜想中一定不成立的是④(填序号);
(2)为确定其它几种猜想是否正确,小明同学进行如表探究:
小亮认为小明实验操作第二步的结论不一定正确,他的理由是酚酞在中性溶液中也是无色的;
(3)请你设计实验方案,确认该溶液是H2SO4溶液,并完成如表实验报告:
【拓展应用】为了防止试剂瓶的标签发生破损,我们在倾倒溶液时应注意:使标签向着手心.
 老师向同学们展示了一瓶标签受损的无色溶液(如图所示),并要求同学们进行探究.
老师向同学们展示了一瓶标签受损的无色溶液(如图所示),并要求同学们进行探究.【提出问题】这瓶无色溶液是什么溶液?
【提出猜想】老师提示:这瓶无色溶液可能是下列四种溶液中的一种:
①MgSO4 ②Na2SO4 ③H2SO4 ④BaSO4
【查阅资料】:Na2SO4的水溶液显中性.
【实验探究】
(1)依据溶解度性,猜想中一定不成立的是④(填序号);
(2)为确定其它几种猜想是否正确,小明同学进行如表探究:
| 实验操作 | 实验现象 | 实验结论 |
| 第一步:取待测溶液少许于试管甲中,向其中滴加几滴NaOH溶液 | 产生白色沉淀 | 猜想①成立 |
| 第二步:另取待测溶液少许于试管乙中,向其中滴加无色酚酞试液 | 无明显现象 | 猜想③成立 |
(3)请你设计实验方案,确认该溶液是H2SO4溶液,并完成如表实验报告:
| 实验操作 | 实验现象 | 实验结论 |
| 取该少许于试管丙中,加入铁粉 | 有气泡产生 | 猜想③成立,该反应的化学方程式为Fe+H2SO4═FeSO4+H2↑ |
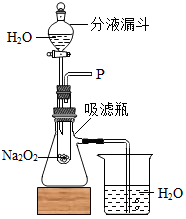 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na2O2)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小军很感兴趣,于是,他和同学们进行探究.
 实验室安如图所示装置制取CO2,并检验CO2的性质.试回答以下问题:
实验室安如图所示装置制取CO2,并检验CO2的性质.试回答以下问题: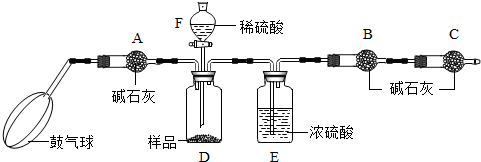
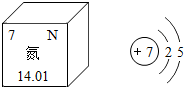 氮在周期表中的信息和原子结构示意图如图.
氮在周期表中的信息和原子结构示意图如图.