题目内容
16.硒对人体有防癌、抗癌作用,如图1是硒元素在元素周期表中的部分信息,图2是硒原子的结构示意图,下列说法错误的是( )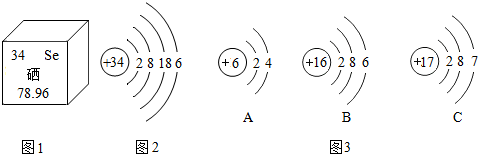
| A. | 硒是人体必需的微量元素 | |
| B. | 由图1可知,硒元素的相对原子质量是78.96 | |
| C. | 图3中A、B、C三种元素中与硒元素化学性质相似的是A元素 | |
| D. | 图3中C元素原子在化学反应中容易得到电子 |
分析 A.根据人体需要的微量元素来分析;
B.根据元素周期表的信息来分析;
C.根据最外层电子数决定元素的化学性质来分析;
D.根据最外层电子数来分析.
解答 解:A.硒是人体必需的微量元素之一,故正确;
B.由元素周期表的信息可知,硒元素的相对原子质量是78.96,故正确;
C.硒元素的原子结构示意图中最外层有6个电子,最外层电子数相同的化学性质相似,故B与硒的化学性质相似;故错误;
D.图3中C元素原子最外层有7个电子,在化学反应中易得到电子,故正确.
故选C.
点评 本题难度不大,考查学生灵活运用元素周期表中元素的信息、原子结构示意图的含义进行分析解题的能力.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案
相关题目
6.呼吸面具中制取氧气的主要原料是固体过氧化钠(Na2O2),某化学兴趣小组的同学为了测定呼吸面具中过氧化钠的质量分数,在老师的指导下,利用如图所示装置(固定装置一略去)开展探究.

已知,装置B 中盛有饱和NaHCO3 溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO 组成的混合物.整套装置气密性良好,反应所需试剂均足量. 2Na2O2+2CO2═2Na2CO3+O2
相关实验数据如下:
(1)装置E的作用为防止空气中的水蒸气、二氧化碳与过氧化钠反应.
(2)根据以上数据计算该样品的纯度.

已知,装置B 中盛有饱和NaHCO3 溶液(NaHCO3不与CO2反应),碱石灰是由固体NaOH和CaO 组成的混合物.整套装置气密性良好,反应所需试剂均足量. 2Na2O2+2CO2═2Na2CO3+O2
相关实验数据如下:
| Na2O2样品的质量/g | D反应前物质的质量/g | D反应后物质的质量/g |
| 40g | 222g | 236g |
(2)根据以上数据计算该样品的纯度.
11.解决大班额,学校添置了很多运动设施或器材,这些器材中没有用到有机合成材料的是( )
| A. |  篮球 | B. |  塑胶跑道 | C. |  钢制单杠 | D. |  尼龙跳绳 |
1.下列实验所对应的方案正确的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别蒸馏水和食盐水 | 取样、加肥皂水 |
| B | 除去CO2气体中的CO | 将混合气体通过足量的氢氧化钠溶液、干燥 |
| C | 区分稀盐酸和稀硫酸 | 加酚酞试液 |
| D | 检验NaOH溶液的变质程度(部分变质还是全部变质) | 加足量BaCl2溶液,过滤,加酚酞 |
| A. | A | B. | B | C. | C | D. | D |
1.实验室里某小组正在探究一个问题.根据设计方案,甲同学向试管中加入2mL氢氧化钠溶液,滴人几滴酚酞溶液,溶液显红色.然后他又用滴管连续滴入一定量的稀硫酸,溶液由红色变为无色.
(1)他们探究的问题是酸和碱溶液能发生中和反应,写出甲同学实验反应的化学方程式:H2SO4+2NaOH═Na2SO4+2H2O
(2)乙同学在滴入几滴酚酞溶液时,溶液变红不是很明显,于是又继续滴加酚酞溶液,却发现溶液由红色褪为无色.
【提出问题】乙同学很诧异,是什么原因导致溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能与所用NaOH溶液浓度较大有关;
乙同学:可能是NaOH溶液与空气中的C02发生了反应;
乙同学的猜想很快被否定,原因是反应生成的碳酸钠溶液显碱性,能使酚酞变红,NaOH溶液与空气中的C02发生反应的化学方程式:2NaOH+CO2═Na2CO3+H2O
【设计实验】(3)甲同学设计了如下实验,请你填写下表.
(4)丙同学根据甲同学的实验结果推测红色褪去的现象与碱溶液无关,可能是所用酚酞溶液的问题.于是他查阅资料,发现酚酞溶液是一种弱有机酸,他又向原氢氧化钠溶液中持续滴加若干滴新配制的酚酞溶液,结果发现溶液变红后并没有消失.这说明酚酞溶液本身微弱的酸性应该不是 (填“是”或“不是”)乙同学实验红色消失的主要原因.
(5)请你再猜测乙同学实验现象的可能原因,并设计实验予以证明(注意:无实验设计证明的不给分).盛酚酞溶液的试剂瓶之前盛过酸溶液没有洗净.取乙同学所用酚酞溶液少许,逐滴滴加氢氧化钠溶液,观察现象.若开始滴加氢氧化钠溶液时无现象,继续滴加后出现红色且不再消失.即可证明..
(1)他们探究的问题是酸和碱溶液能发生中和反应,写出甲同学实验反应的化学方程式:H2SO4+2NaOH═Na2SO4+2H2O
(2)乙同学在滴入几滴酚酞溶液时,溶液变红不是很明显,于是又继续滴加酚酞溶液,却发现溶液由红色褪为无色.
【提出问题】乙同学很诧异,是什么原因导致溶液由红色褪为无色?
【猜想与假设】他们分别对这种意外现象作如下猜想:
甲同学:可能与所用NaOH溶液浓度较大有关;
乙同学:可能是NaOH溶液与空气中的C02发生了反应;
乙同学的猜想很快被否定,原因是反应生成的碳酸钠溶液显碱性,能使酚酞变红,NaOH溶液与空气中的C02发生反应的化学方程式:2NaOH+CO2═Na2CO3+H2O
【设计实验】(3)甲同学设计了如下实验,请你填写下表.
| 实验步骤 | 实验现象 | 实验结论 |
| 1将NaOH溶液稀释,滴人该酚酞溶液. | 溶液变红,继续滴加酚酞溶液,红色消失 | 甲同学猜想不正确 (填“正确”或“不正确”) |
| 2向澄清石灰水中滴入该酚酞溶液 |
(5)请你再猜测乙同学实验现象的可能原因,并设计实验予以证明(注意:无实验设计证明的不给分).盛酚酞溶液的试剂瓶之前盛过酸溶液没有洗净.取乙同学所用酚酞溶液少许,逐滴滴加氢氧化钠溶液,观察现象.若开始滴加氢氧化钠溶液时无现象,继续滴加后出现红色且不再消失.即可证明..

 ”)表示相连物质间可以反应,“→”表示物质间可以转化(注:反应条件、部分反应物或生成物略去).
”)表示相连物质间可以反应,“→”表示物质间可以转化(注:反应条件、部分反应物或生成物略去).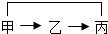 ,甲、乙、丙为不同类别的化合物,甲→乙、乙→丙均为复分解反应,则甲与丙反应的化学方程式为Ca(OH)2 +CO2═CaCO3↓+H2O.
,甲、乙、丙为不同类别的化合物,甲→乙、乙→丙均为复分解反应,则甲与丙反应的化学方程式为Ca(OH)2 +CO2═CaCO3↓+H2O.