题目内容
7.氢气是最轻的气体,难溶于水.氢气作为未来的理想能源,是航天工业的高能燃料,也是化工生产的重要原料.实验室通常采用如图装置制取少量氢气,请根据要求回答:
①实验室使用稀盐酸和金属锌制取氢气的化学反应方程式为Zn+2HCl=ZnCl2+H2↑,这种方法制得的氢气往往含有少量氯化氢(原因是盐酸具有挥发性)和水蒸气,可将杂质气体通过装置B、C除去;
②实验中可采用E、F装置收集氢气;集满氢气后的集气瓶按装置G方式放置备用,原因是氢气比空气轻,防止逸出.
分析 (1)根据锌与稀盐酸反应生成氯化锌和氢气,根据B装置中氢氧化钠的性质、浓硫酸具有吸水性分析除掉的杂质;
(2)根据氢气的物理性质特别是密度比空气小以及难溶于水分析判断.
解答 解:(1)锌与稀盐酸反应生成氯化锌及氢气,化学方程式为:Zn+2HCl=ZnCl2+H2↑,盐酸易挥发,所以这种方法制得的氢气往往含有少量氯化氢和水蒸气,由于B装置中氢氧化钠能与氯化氢反应,所以可除掉气体中的氯化氢气体,装置C中浓硫酸具有吸水性,可除去水蒸气;
(2)由于氢气密度比空气小,所以可采用向下排空气法收集,且集满氢气后的集气瓶应倒放到桌面上,氢气难溶于水,所以也可采用排水法收集.
故答案为:(1)Zn+2HCl=ZnCl2+H2↑,氯化氢,盐酸具有挥发性,水蒸气,B、C;
(2)E、F,氢气比空气轻,防止逸出.
点评 本题是对氢气制取及除杂的考查,解题的关键是掌握相关物质的性质,属基础性知识考查题.

练习册系列答案
 互动英语系列答案
互动英语系列答案
相关题目
15.下列物质的溶液,需要另加试剂才能鉴别出来的一组是( )
| A. | CuSO4 BaCl2 H2SO4 | B. | Na2CO3 Ca(NO3)2 HCl | ||
| C. | Na2SO4 KNO3 HCl | D. | FeCl2 NaOH KMnO4 |
12.甲、乙、丙是初中学习过的物质,甲在发生化合反应时能生成乙或丙,乙、丙两种物质能相互转化.则下列说法正确的是( )
| A. | 甲可能是O2 | B. | 甲一定是H2 | C. | 乙可能是H2O | D. | 丙一定是CO |
19.推理是学习化学的重要方法之一,下列推理正确的是( )
| A. | 碱溶液显碱性,所以显碱性的溶液一定是碱溶液 | |
| B. | 向某固体中加稀盐酸,产生无色无味气体,则该物质中一定含CO32+或HCO3- | |
| C. | 某物质在氧气中燃烧生成二氧化碳和水,则该物质中一定含碳、氢、氧三种元素 | |
| D. | 单质中只含一种元素,因此只含一种元素的纯净物一定是单质 |
16.硒对人体有防癌、抗癌作用,如图1是硒元素在元素周期表中的部分信息,图2是硒原子的结构示意图,下列说法错误的是( )
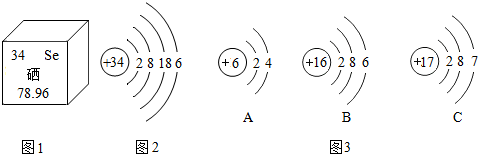

| A. | 硒是人体必需的微量元素 | |
| B. | 由图1可知,硒元素的相对原子质量是78.96 | |
| C. | 图3中A、B、C三种元素中与硒元素化学性质相似的是A元素 | |
| D. | 图3中C元素原子在化学反应中容易得到电子 |