题目内容
7.钙元素是一种重要的金属元素,它形成的物质种类很多.(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂.
某实验探究小组的通许通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是放热(填“吸热”或“放热”),实验室可以用pH试纸测定其溶液的酸碱度.
(3)实验探究小组将Na2CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【做出猜想】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是因为氢氧化钙和碳酸钠不能共存.
【实验过程】
| 实验步骤 | 现象 | 结论 |
| 实验Ⅰ:取滤液,向其中滴入适量Na2CO3溶液 | 没有明显现象 | 猜想二不成立 |
| 实验Ⅱ:另取滤液,向其中加入足量 稀盐酸 | 产生气泡 | 猜想 三成立 |
分析 (1)根据氢化钙(CaH2)遇水反应生成氢氧化钙和氢气,写出该反应的化学方程式即可;
(2)根据生石灰与水反应放出大量的热进行分析;根据溶液酸碱度的测定方法进行分析;
(3)根据实验研究的方法和物质间的反应规律分析.
解答 解:(1)氢化钙(CaH2)遇水反应生成氢氧化钙和氢气,化学化学方程式:CaH2+2H2O═Ca(OH)2+2H2↑;
故填:CaH2+2H2O═Ca(OH)2+2H2↑;
(2)生石灰与水反应生成氢氧化钙,反应放出大量的热;溶液的酸碱度可以用pH试纸来测定;
故填:放热;pH试纸;
(3)猜想假设:
氢氧化钙和碳酸钠反应时,可能恰好完全反应,这时的滤液中含有的溶质是氢氧化钠;
如果氢氧化钙过量时,滤液中含有的溶质是氢氧化钠和氢氧化钙;
如果碳酸钠过量时,滤液中含有的溶质是氢氧化钠和碳酸钠.
猜想四的猜想肯定是不合理的,因为氢氧化钙和碳酸钠不能共存.
故【做出猜想】填:Na2CO3.因为氢氧化钙和碳酸钠不能共存;
实验步骤:实验Ⅰ:取滤液,向其中滴入适量Na2CO3,如没有明显现象,说明没有氢氧化钙,则证明猜想二不成立;实验Ⅱ:另取滤液,向其中加入足量稀盐酸,产生气泡,则说明有Na2CO3,证明猜想三成立;
故填:没有明显现象;稀盐酸;三.
【拓展延伸】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑原反应的物质是否过量;
故填:原反应的物质是否过量.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.下列知识整理正确的一组是( )
| A、物质组成 | B、化学与生活 |
| ●消石灰、生石灰-化学式都是Ca(OH)2 ●蔗糖、葡萄糖、淀粉-都属于糖类物质 | ●除餐具上的油污-用洗洁精溶解 ●棉织物、羊毛织物-用灼烧闻气味来鉴别 |
| C、实验记录 | D、食品与健康 |
| ●用广泛pH试纸测定出某溶液pH值为4.2 ●用量筒量取5.25毫升水 | ●重金属中毒--喝牛奶解毒 ●人体缺碘--多吃海带、紫菜 |
| A. | A | B. | B | C. | C | D. | D |
18.下列实验操作中正确的是( )
| A. | 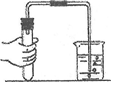 检查气密性 | B. | 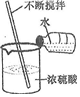 浓硫酸的稀释 | C. | 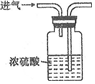 干燥氧气 | D. | 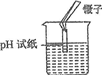 测定某溶液的pH |
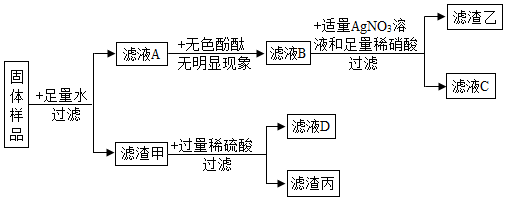
15.娄底人在端午节有吃皮蛋的习俗.某化学小组的同学查阅资料后得知,腌制皮蛋的主要原料有:生石灰、纯碱和食盐.同学们向这三种物质中加入适量水,充分搅拌,过滤,对滤渣中溶质的成分进行探究.
小组同学讨论后一致认为,滤液中的溶质一定含有NaCl和NaOH.(写化学式)
【提出问题】滤液中还可能含有哪些溶质呢?
【作出猜想】
小林认为:还含有Ca(OH)2
小方认为:还含有Na2CO3
小华认为:还含有Ca(OH)2和Na2CO3
【交流讨论】经过进一步讨论,大家认为小华的猜想不合理,原因是:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.(用化学方程式表示)
【实验探究】
【交流谈论】同学们认为,通过小华的实验不足以得出其结论,原因是小华的实验不能证明滤液中是否含有碳酸钠.
【继续探究】小明也取少量滤液于试管中,滴加稀盐酸,却没有看到明显现象,小明对此深感疑惑.
【解释评价】经老师的指导和大家的认真思考后终于找出了原因,你认为是小明加入的稀盐酸的量不足,氢氧化钠先与少量的稀盐酸反应生成氯化钠和水.最后,老师对同学们这种严谨的科学态度给予了充分的肯定.
小组同学讨论后一致认为,滤液中的溶质一定含有NaCl和NaOH.(写化学式)
【提出问题】滤液中还可能含有哪些溶质呢?
【作出猜想】
小林认为:还含有Ca(OH)2
小方认为:还含有Na2CO3
小华认为:还含有Ca(OH)2和Na2CO3
【交流讨论】经过进一步讨论,大家认为小华的猜想不合理,原因是:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.(用化学方程式表示)
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 小林:取少量滤液于试管中,滴加足量的稀盐酸 | 有气泡产生 | 小方的猜想正确 |
| 小方:取少量滤液于试管中,滴加 足量的澄清石灰水溶液 | 产生白色沉淀 | 小方的猜想正确 |
| 小华:取少量滤液于试管中,滴加Na2CO3溶液 | 无明显现象 | 小方的猜想正确 |
【继续探究】小明也取少量滤液于试管中,滴加稀盐酸,却没有看到明显现象,小明对此深感疑惑.
【解释评价】经老师的指导和大家的认真思考后终于找出了原因,你认为是小明加入的稀盐酸的量不足,氢氧化钠先与少量的稀盐酸反应生成氯化钠和水.最后,老师对同学们这种严谨的科学态度给予了充分的肯定.
12.下列化学反应属于关系图中阴影部分的是( )


| A. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | B. | CO+CuO$\frac{\underline{\;加热\;}}{\;}$Cu+CO2 | ||
| C. | CaO+H2O═Ca(OH)2 | D. | 2NaOH+H2SO4=Na2SO4+2H2O |
16.下列关于实验现象的描述不正确的是( )
| A. | 将生铁粉末投入盛有过量盐酸的烧杯中,充分反应后仍有黑色残渣 | |
| B. | 硫在空气中燃烧发出淡蓝色的火焰 | |
| C. | 家庭小实验中,将食醋与纯碱混合有大量气泡产生 | |
| D. | 铁丝在氧气中燃烧发出白光,生成黑色固体 |