题目内容
2.A---I是初中化学常见物质,已知A、E为红色粉末,C、G是黑色粉末,B、H是气体且B是化合物,D溶液呈蓝色,可用于配制农药波尔多液,它们之间的转化关系如图(各步均恰好完全反应),请回答下列问题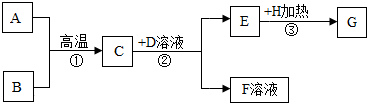
(1)F的化学式是FeSO4(2)反应①的化学方程式3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
(3)反应③的基本反应类型为化合反应(4)写出B物质的一种用途气体燃料(或冶炼金属).
分析 根据题干提供的信息进行分析解答,D溶液呈蓝色,可用于配制农药波尔多液,故D是硫酸铜溶液;A为红色粉末,C是黑色粉末,B、H是气体且B是化合物,故A和B的反应是氧化铁与一氧化碳的反应,A是氧化铁,B是一氧化碳,生成的C是铁,铁能与硫酸铜反应生成硫酸亚铁和铜,E为红色粉末E是铜,铜能与H加热反应生成黑色粉末G,故G是氧化铜,据此解答.
解答 解:(1)F是硫酸亚铁,故填:FeSO4;
(2)一氧化碳能与氧化铁高温反应生成铁和二氧化碳,故填:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)反应③是铜和氧气的反应,属于化合反应,故填:化合反应;
(4)B是一氧化碳,具有可燃性和还原性,可以用作燃料,用于冶炼金属,故填:气体燃料(或冶炼金属).
点评 此题为框图式物质推断题,完成此类题目,关键是找准解题突破口,直接得出结论,然后利用顺向或逆向或两边向中间推,逐一导出其他结论,本题的开放度较大,不必拘泥于面面俱到,只要符合题意即可.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
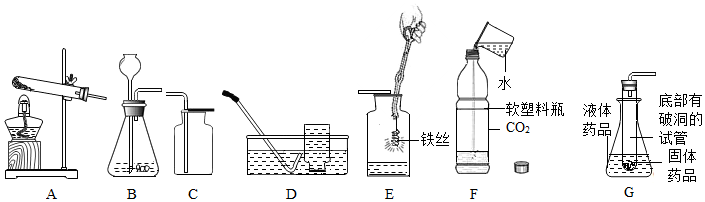
12. (1)如图是实验室制取气体的一些装置,据图回答:
(1)如图是实验室制取气体的一些装置,据图回答:
①图B中仪器a的名称是铁架台
②用高锰酸钾制取氧气的发生装置是A(填序号),若用C装置收集氧气,验满时,应将带火星的木条放在c(填“b”或“c”)端导管口,若木条复燃,说明氧气已满.
(2)小明在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究.
[查阅资料]:①KOH与NaOH的化学性质相似.请用化学方程式解释KOH变质的原因是CO2+2KOH═K2CO3+H2O.
②K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性.
[猜想假设]:假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3
[进行实验]:
[问题讨论]:步骤②中加入过量BaCl2溶液的作用是除去样品中的碳酸钾
[拓展应用]:完全变质的KOH也有利用价值,从K2CO3组成或性质看,这瓶变质的试剂在农业上的用途是作钾肥.
 (1)如图是实验室制取气体的一些装置,据图回答:
(1)如图是实验室制取气体的一些装置,据图回答:①图B中仪器a的名称是铁架台
②用高锰酸钾制取氧气的发生装置是A(填序号),若用C装置收集氧气,验满时,应将带火星的木条放在c(填“b”或“c”)端导管口,若木条复燃,说明氧气已满.
(2)小明在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其成分提出以下假设,并在老师的指导下进行实验探究.
[查阅资料]:①KOH与NaOH的化学性质相似.请用化学方程式解释KOH变质的原因是CO2+2KOH═K2CO3+H2O.
②K2CO3溶液呈碱性,BaCl2溶液、KCl溶液呈中性.
[猜想假设]:假设Ⅰ:只含KOH;假设Ⅱ:含KOH和K2CO3;假设Ⅲ:只含K2CO3
[进行实验]:
| 实验操作步骤 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入足量的稀盐酸 | 有气泡产生 | 假设Ⅰ不正确 |
| ②另取少量样品于试管中,加水溶解,加入过量的BaCl2溶液,振荡,静置 | 产生白色沉淀 | 假设Ⅲ正确 |
| ③取②中上层清液,滴加无色酚酞溶液 | 无色酚酞溶液不变色 |
[拓展应用]:完全变质的KOH也有利用价值,从K2CO3组成或性质看,这瓶变质的试剂在农业上的用途是作钾肥.
17.下列对实验现象的描述正确的是( )
| A. | 红磷在空气中燃烧,产生大量的白雾 | |
| B. | 铁丝浸入稀盐酸,形成黄色溶液 | |
| C. | 持续加热碳酸氢钠,最终没有固体残留 | |
| D. | 向氢氧化钠溶液中加入硫酸铜溶液有蓝色沉淀生成 |
7.钙元素是一种重要的金属元素,它形成的物质种类很多.
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂.
某实验探究小组的通许通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是放热(填“吸热”或“放热”),实验室可以用pH试纸测定其溶液的酸碱度.
(3)实验探究小组将Na2CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【做出猜想】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是因为氢氧化钙和碳酸钠不能共存.
【实验过程】
【拓展延伸】在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑原反应的物质是否过量.
(1)氢化钙(CaH2)固体是登山运动员常用的能源提供剂.
某实验探究小组的通许通过查阅资料得知:CaH2能与H2O反应生成Ca(OH)2和H2,请你写出该反应的化学方程式CaH2+2H2O═Ca(OH)2+2H2↑.
(2)生石灰溶于水可制得熟石灰,该反应过程中能量的变化是放热(填“吸热”或“放热”),实验室可以用pH试纸测定其溶液的酸碱度.
(3)实验探究小组将Na2CO3溶液滴加到Ca(OH)2溶液中,充分反应后过滤,得到滤渣和滤液,经检验滤渣的成分是碳酸钙.
【提出问题】滤液中溶质的成分是什么?
【做出猜想】
猜想一:NaOH 猜想二:NaOH和Ca(OH)2
猜想三:NaOH和Na2CO3 猜想四:NaOH、Na2CO3和Ca(OH)2
经过讨论,大家认为猜想四不合理,原因是因为氢氧化钙和碳酸钠不能共存.
【实验过程】
| 实验步骤 | 现象 | 结论 |
| 实验Ⅰ:取滤液,向其中滴入适量Na2CO3溶液 | 没有明显现象 | 猜想二不成立 |
| 实验Ⅱ:另取滤液,向其中加入足量 稀盐酸 | 产生气泡 | 猜想 三成立 |
11.南京青奥会火炬使用的燃料为A物质,纯净物A在B物质中充分燃烧,发生反应为A+5B$\frac{\underline{\;点燃\;}}{\;}$3C+4D(部分微观示意图如图所示).
(1)上述反应中A物质的化学式为C3H8.
(2)反应过程中A物质与B物质的质量比为11:40.
| 物质 | A | B | C | D | 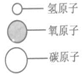 |
| 分子示意图 | ? |  |  |  |
(2)反应过程中A物质与B物质的质量比为11:40.
12.2017年5月18日,国土资源部宣布:我国首次(也是世界首次)在南海成功试采海域可燃冰.可燃冰的主要成分是( )
| A. | 甲烷水合物 | B. | 一氧化碳 | C. | 氢气 | D. | 氮气 |
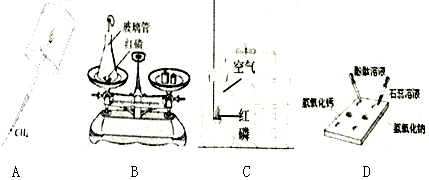
 (1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.
(1)做实验时要严格遵守实验室规则.请写出“题19图”这些同学做化学实验时的违规行为(写三点):①在实验室内追逐打闹;②在实验室里吃喝食物(或尝药品的味道);③用手直接拿着试管加热.