题目内容
2.某金属冶炼厂的管道烟泥中含有某些单质,其中Cu约占10.3%、Zn约占5.0%、S约占1.2%.现欲回收铜和锌,并对硫进行环保处理,主要步骤如图所示:
已知:加热的条件下,Zn、Cu都可以与氧气反应生成相应的金属氧化物;
ZnO+H2SO4═ZnSO4+H2O;CuO+H2SO4═CuSO4+H2O
(1)步骤①产生的废气A中,一定含有的有害气体是二氧化硫(SO2).
(2)步骤③中反应的化学方程式是Zn+CuSO4═ZnSO4+Cu、Zn+H2SO4═ZnSO4+H2↑.
(3)下列说法正确的是ad.
a.②、③中的操作均包含过滤
b.溶液D和溶液F中ZnSO4的质量相等
c.溶液D中ZnSO4的质量大于CuSO4的质量
d.若步骤①中空气不足量,不会导致锌的回收率降低.
分析 (1)因为烟泥中含有硫的单质,故加热后会生成有毒气体二氧化硫.
(2)通过生成物的分析可以看出甲是锌反应时会置换出铜,并消耗溶液中的剩余硫酸.
(3)a、过滤是把固体和液体分开的操作;b、溶液F中比溶液D中增多了ZnSO4;c、Cu约占10.3%、Zn约占5.0%、溶液D中ZnSO4的质量不会大于CuSO4的质量;
d、空气量不足不会影响锌的回收,因为不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收.
解答 解:(1)烟泥中存在单质硫,在空气中加热时会产生二氧化硫,二氧化硫是常见的空气污染物.
故答案为:二氧化硫(SO2);
(2)由于生成物是铜与硫酸锌可知甲是锌,过量的锌除置换铜外还会消耗溶液中的剩余硫酸,所以会发生两个反应,即锌与硫酸铜、锌与硫酸.
故答案为:Zn+CuSO4═ZnSO4+Cu、Zn+H2SO4═ZnSO4+H2↑
(3)a、过滤是把固体和液体分开的操作,故A对;
b、溶液F中比溶液D中增多了ZnSO4,故B错;
c、Cu约占10.3%、Zn约占5.0%、溶液D中ZnSO4的质量不会大于CuSO4的质量,故C错;
d、空气量不足不会影响锌的回收,因为不管锌在第一步中是否被氧化,在第二步中都会完全转化为硫酸锌,不会影响锌的回收,故D对.
故选ad.
故答案为:(1)二氧化硫(SO2);
(2)Zn+H2SO4 ZnSO4+H2↑;Zn+CuSO4 ZnSO4+Cu;
(3)ad.
点评 此题是对物质分离与提纯的知识的考查,解决的重点是对每一步具体的反应做出详细的分析与判断,属基础性知识考查题.

练习册系列答案
 阳光课堂课时作业系列答案
阳光课堂课时作业系列答案
相关题目
12.甲、乙两物质发生反应的微观示意图如图,则下列说法中,不正确的是( )


| A. | 该反应属于化合反应 | B. | 该反应前后原子个数保持不变 | ||
| C. | 该反应遵循质量守恒定律 | D. | 甲和丙中同种元素的化合价均相等 |
10.下列有关溶解、溶液的说法中不正确的是( )
| A. | 用汽油、洗涤剂都能洗去油污,二者都是利用溶解作用 | |
| B. | 从5%的蔗糖溶液中取出1滴,这1滴溶液的浓度仍为5% | |
| C. | 酸、碱、盐的溶液能导电,是因为溶液中存在自由移动的离子 | |
| D. | 在配制溶液时,所用的溶质可以是固体、液体,也可以是气体 |
17.下列物质露置在潮湿的空气中一段时间后,质量不会增加的是( )
| A. | 浓硫酸 | B. | 铁粉 | C. | 烧碱 | D. | 浓盐酸 |
7.下列图象能正确反映对应变化关系的是( )
| A. |  向一定量稀硫酸中加入NaOH溶液 | |
| B. |  向一定量稀盐酸中加入铁粉 | |
| C. |  向一定量CaCl2、CaCO3固体混合物中加入稀盐 | |
| D. | 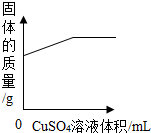 向一定量铁粉中加入CuSO4溶液 |
14.为研究NaOH与盐酸的反应,同学们用以下试剂设计不同方案进行探究.
实验试剂:镁条、蒸馏水、稀盐酸、NaOH溶液、NaCl溶液等
(1)小明取少量NaOH溶液于试管中,滴入酚酞,溶液变红,再滴加稀盐酸,振荡,红色褪去,可推断NaOH与盐酸发生了反应.反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)小刚取体积相同的稀盐酸分别于甲、乙两支试管中,向甲中先加1mL水,充分混合后再放入镁条,向乙中先加入1mL NaOH溶液,充分混合后再放入镁条.观察到甲中有气泡冒出,乙中无气泡(或气泡少),可推断NaOH与盐酸发生了反应.
(3)小华利用溶液导电性进行实验.分别测定几种试剂的导电性,获得相关数据:
查阅资料:
Ⅰ.溶液中若存在自由移动的离子,通电时就会发生定向移动,从而形成了电流.
Ⅱ.相同电压下,等体积溶液中,所含离子数目越多,电流就越大.
①对比实验A、C的数据,可推知NaOH溶液中除水分子外还含有自由移动的Na+和OH-(填化学符号).
②实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等(填写“相等”或“不相等”).
③各取10mL NaOH溶液于两个小烧杯中,分别加入10mL NaCl溶液和10mL稀盐酸(所得混合溶液体积均约为20mL),测两种混合溶液的导电性,电流示数依次为I1和I2.根据I1> I2(填“>”、“<”或“=”),也可推断氢氧化钠和盐酸发生了反应.
实验试剂:镁条、蒸馏水、稀盐酸、NaOH溶液、NaCl溶液等
(1)小明取少量NaOH溶液于试管中,滴入酚酞,溶液变红,再滴加稀盐酸,振荡,红色褪去,可推断NaOH与盐酸发生了反应.反应的化学方程式为NaOH+HCl═NaCl+H2O.
(2)小刚取体积相同的稀盐酸分别于甲、乙两支试管中,向甲中先加1mL水,充分混合后再放入镁条,向乙中先加入1mL NaOH溶液,充分混合后再放入镁条.观察到甲中有气泡冒出,乙中无气泡(或气泡少),可推断NaOH与盐酸发生了反应.
(3)小华利用溶液导电性进行实验.分别测定几种试剂的导电性,获得相关数据:
| 实验序号 | A | B | C | D |
| 试剂 | 蒸馏水 | 稀盐酸 | NaOH溶液 | NaCl溶液 |
| 电流强度/mA | 约为0 | 0.09 | 0.09 | 0.09 |
Ⅰ.溶液中若存在自由移动的离子,通电时就会发生定向移动,从而形成了电流.
Ⅱ.相同电压下,等体积溶液中,所含离子数目越多,电流就越大.
①对比实验A、C的数据,可推知NaOH溶液中除水分子外还含有自由移动的Na+和OH-(填化学符号).
②实验B、D中电流强度相等,说明等体积的稀盐酸和NaCl溶液中所含Cl-的数目相等(填写“相等”或“不相等”).
③各取10mL NaOH溶液于两个小烧杯中,分别加入10mL NaCl溶液和10mL稀盐酸(所得混合溶液体积均约为20mL),测两种混合溶液的导电性,电流示数依次为I1和I2.根据I1> I2(填“>”、“<”或“=”),也可推断氢氧化钠和盐酸发生了反应.
11.下列日常学习生活中的做法正确的是( )
| A. | 坚持只喝纯净水 | B. | 把浓硫酸倒入盛有水的量筒里稀释 | ||
| C. | 进入深洞时要带电筒还要打火把 | D. | 用亚硝酸钠代替食盐作调味品 |
3.ClO2是优良的饮用水消毒剂.ClO2中氯元素的化合价是( )
| A. | +5 | B. | +4 | C. | +2 | D. | -1 |
 在做完常见酸碱盐性质的实验后,课外小组的同学帮助老师整理实验用品,发现有一个失去标签的试剂瓶(如图),里面盛有无色、无味的液体,老师建议他们通过实验方法给予确认,大家进行了讨论和探究.请你也来参与吧.
在做完常见酸碱盐性质的实验后,课外小组的同学帮助老师整理实验用品,发现有一个失去标签的试剂瓶(如图),里面盛有无色、无味的液体,老师建议他们通过实验方法给予确认,大家进行了讨论和探究.请你也来参与吧.