题目内容
15.下列各组物质为同一种物质的是( )| A. | NaOH氢氧化钠纯碱 | B. | CO2二氧化碳干冰 | ||
| C. | NaHCO3碳酸钠苏打 | D. | CaO 氢氧化钙消石灰 |
分析 根据物质的物质名称、俗名以及化学式分析解答.
解答 解:A.氢氧化钠俗称烧碱、火碱、苛性钠,而纯碱是碳酸钠的俗称,故错误;
B.固态的二氧化碳俗称干冰,故正确;
C.NaHCO3是碳酸氢钠的化学式,俗称小苏打,故错误;
D.氢氧化钙的化学式为Ca(OH)2,CaO是氧化钙的化学式,故错误.
故选B.
点评 本题主要考查物质的物质名称、俗名以及化学式,难度不大.

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
5. 某同学为了探究氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:
某同学为了探究氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:
【实验一】实验目的:探究氧化铜是否能改变过氧化氢分解的速率.
结论:氧化铜能加快过氧化氢的分解速率.
【实验二】实验目的:探究氧化铜的化学性质在化学反应前后是否发生了改变
结论:氧化铜的化学性质在化学反应前后没有发生改变.
【实验三】实验目的:探究氧化铜的质量在化学反应前后有没有改变.
在实验后,该同学将反应剩余物过滤、洗涤、干燥,再称量,得到黑色固体质量为1g.
结论:氧化铜的质量在化学反应前后没有发生改变.
【实验结论】综上所述,说明了氧化铜是过氧化氢溶液分解的催化剂.请写出该实验中过氧化氢溶液分解反应的化学方程式2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
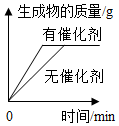
某同学画出如图,表示有、无催化剂时,生成物质量与反应时间的关系图,你认为是否正确?正确.
 某同学为了探究氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:
某同学为了探究氧化铜(难溶于水)是否能做过氧化氢(H2O2)分解制取氧气的催化剂,设计实验如下:【实验一】实验目的:探究氧化铜是否能改变过氧化氢分解的速率.
| 1.在试管中加入2ml5%的过氧化氢溶液,将带火星的木条伸入试管中,观察现象. | 1.带火星的木条没有明显变化 |
| 2.取1gCuO粉末放在放在步骤1中的试管中,振荡,把带火星的木条伸入试管中 | 2.带火星的木条复燃 |
【实验二】实验目的:探究氧化铜的化学性质在化学反应前后是否发生了改变
| 实验步骤 | 实验现象 |
| 待实验一第2步的试管中没有气泡时,重新加入2ml过氧化氢溶液,观察现象. | 试管中有大量的气泡冒出 |
【实验三】实验目的:探究氧化铜的质量在化学反应前后有没有改变.
在实验后,该同学将反应剩余物过滤、洗涤、干燥,再称量,得到黑色固体质量为1g.
结论:氧化铜的质量在化学反应前后没有发生改变.
【实验结论】综上所述,说明了氧化铜是过氧化氢溶液分解的催化剂.请写出该实验中过氧化氢溶液分解反应的化学方程式2H2O2$\frac{\underline{\;CuO\;}}{\;}$2H2O+O2↑.
某同学画出如图,表示有、无催化剂时,生成物质量与反应时间的关系图,你认为是否正确?正确.
10.填写实验报告.
| 实验内容 | 实验现象 | 实验结论 |
| (1)用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻 | 蘸酒精的棉花燃烧. | 通过此实验,可以说明燃烧的条件之一是:燃烧需要可燃物. |
(2)从乒乓球和滤纸上各剪下一小片(同样大小),如图分别放在薄铜片的两侧,加热铜片的中部,观察现象.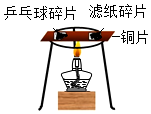 | 乒乓球碎片先燃烧. | 通过此实验,可以说明燃烧的条件之一是:温度需要可燃物的着火点. |
(3)点燃两支蜡烛,在其中一支蜡烛上倒扣一个A烧杯,另一支蜡烛放在B烧杯中.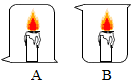 | A烧杯中蜡烛 熄灭,B烧杯中蜡烛正常燃烧. | 通过此实验,可以说明燃烧的条件之一是:可燃物要与氧气接触. |
4.据报道北京2016年12月出现了严重雾霾天气,多次启动空气重污染红色预警,实行机动车单双号行驶、中小学幼儿园停课等措施.下列做法不会加剧雾霾天气形成的是( )
| A. | 机动车辆排放尾气 | B. | 露天焚烧垃圾 | ||
| C. | 城市绿化 | D. | 工厂排放烟尘 |
5.下列关于化学实验的“目的-操作-现象-结论”的描述正确的是( )
| 选项 | 实验目的 | 所加试剂(或操作) | 实验现象 | 实验结论 |
| A | 检验某混合气体中是否含有CO2气体 | 通入澄清石灰水中 | 无明显现象 | 该气体中不含CO2 |
| B | 区分硬水和软水 | 肥皂水 | 产生大量泡沫 | 该液体为蒸馏水 |
| C | 用排空气法收集CO2时检验集气瓶中CO2是否集满 | 将燃烧的木条伸入瓶内 | 木条熄灭 | 瓶内CO2已集满 |
| D | 检验某混合气体中是否含有CO气体 | 通入灼热氧化铜中 | 固体由黑色变为红色 | 该气体中可能含有CO |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
 如图所示装置可用来测量生成的气体的体积.
如图所示装置可用来测量生成的气体的体积. 化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.如图A,检查装置的气密性,操作为将导管末端浸入水中,用手或热毛巾捂热试管,观察到导管口有气泡冒出.然后加入药品,固定装置,制取CO2,有关化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
化学兴趣小组的同学设计并进行了CO2的制取与性质的实验.如图A,检查装置的气密性,操作为将导管末端浸入水中,用手或热毛巾捂热试管,观察到导管口有气泡冒出.然后加入药品,固定装置,制取CO2,有关化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.


