题目内容
17.小红发现切开的苹果会很快变色,于是在老师的指导下,探究氧气是否参与了苹果变色的过程.小红提出假设:氧气参与了苹果变色的过程.老师指导小红要进行对比实验,小红设计并完成了如下2个实验.(1)实验1:探究使苹果变色的气体成分.
实验步骤:
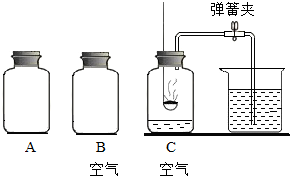
①准备如下图所示的实验装置,A为用排水集气法收集的1瓶氧气,B为1瓶空气,C瓶中为空
气,3个集气瓶容积均为250mL;
②在C瓶中做红磷燃烧的实验,待冷却至室温后打开弹簧夹,至水不再进入集气瓶中,测量进入集气瓶中水的体积约为50mL,剩余气体的主要成分为氮气;
③将大小相同的苹果块依次迅速放入集气瓶A、B和C中,记录苹果的变色时间.
| A | B | C | |
| 放入苹果起始时间 | 下午2:00 | 下午2:00 | 下午2:00 |
| 实验现象 | 下午2:03 苹果变色 | 下午2:09 苹果变色 | 下午2:19 苹果未变色 |
(2)实验2:探究苹果变色消耗的气体体积.
小红为了探查集气瓶A、B中消耗气体的体积,她采取的实验步骤是:分别在AB两瓶中做白磷燃烧实验,待冷却至室温后打开弹簧夹,至水不再进入集气瓶中,测量进水的体积便知白磷消耗氧气的体积.
实验后小红记录了进入集气瓶内水的体积,由此计算出A瓶中消耗气体的体积,请你在表格中填写B瓶消耗气体的体积中.
| A | B | |
| 进入水的体积 | 200mL | 42mL |
| 消耗气体的体积 | 50mL | 8mL |
分析 (1)①根据探究该实验的目的:“探究氧气是否参与了苹果变色的过程”,所以缺少一瓶氧气;
②根据C瓶中红磷燃烧消耗掉氧气,剩余的主要是氮气;
结论:根据A、B瓶内有氧气,C瓶内没氧气,且有氧气的苹果都变色,比较即可得出苹果变色与氧气有关;
(2)分别在AB两瓶中做白磷燃烧实验,待冷却至室温后打开弹簧夹,至水不再进入集气瓶中,测量进水的体积便知白磷消耗氧气的体积.进而求算出苹果消耗的氧气;
(3)根据用红磷测量空气中氧气的含量分析注意事项.
解答 解:(1)①因为实验的目的是探究氧气是否参与了苹果变色的过程,所以需要一瓶氧气.
故答案为:氧气;
②红磷燃烧消耗掉氧气,所以瓶内的气体是氮气.
故答案为:氮气;
③由于A、B瓶内有氧气,C瓶内没氧气,且A、B瓶内苹果变色.
故答案为:苹果变色与氧气有关;
(2)由于A瓶是250mL纯氧气,进入水是200mL,说明苹果消耗了50mL氧气.B瓶内是250mL空气,氧气的含量是250mL×$\frac{1}{5}$=50mL,而进入的水是42mL,说明苹果消耗氧气的体积为:50mL-42mL=8mL,
故答案为:分别在AB两瓶中做白磷燃烧实验,待冷却至室温后打开弹簧夹,至水不再进入集气瓶中,测量进水的体积便知白磷消耗氧气的体积;8;
(3)本实验的导致测量的结果不够准确的原因与红磷的量,装置的气密性等有关.
故答案为:装置的气密性不好.
点评 本题通过设计实验验证苹果的变色与氧气有关,也通过实验验证了消耗氧气的体积,通过实验的设计考查了学生的自主创新的思维和动手实验的能力.

练习册系列答案
相关题目
7.下面O2和CO2的自述中,属于或利用了物理性质的是( )
| A. |  | B. |  | ||
| C. |  | D. |  |
8.下列各组物质同时加入水中,能大量共存的无色溶液是( )
| A. | NaCl、BaCl2、CuSO4、KNO3 | B. | NaCl、Na2CO3、KNO3、KCl | ||
| C. | NaOH、FeCl3、MgSO4、KCl | D. | Ba(NO3)2、NaCl、H2SO4、HCl |
5.将FeSO4 在固体状态下转化成Fe(OH)SO4的方法来制取新型净水剂碱式硫酸铁混凝剂.其中生产过程可以用4FeSO4+2H2O+X=Fe(OH)SO4 表示,则X的化学式为( )
| A. | SO2 | B. | SO2 | C. | FeO | D. | O2 |
6.下列关于空气的说法中错误的是( )
| A. | 空气是人类宝贵的自然资源 | |
| B. | 空气中的氮气常用作保护气 | |
| C. | 空气中的稀有气体常用作灭火剂 | |
| D. | 空气中稀有气体都没有颜色、没有气味,在通电时能发出不同颜色的光 |
 人的胃酸过多,会引起胃病.如图所示是某抗酸药标签上的部分文字.某同学为了测定该药中氢氧化铝的质量分数,进行如下操作:取一片药片(药片质量0.5g),研碎后加20mL蒸馏水,然后用质量分数为5%的盐酸至反应完全(其他成分不与盐酸反应),测定实验中反应掉的盐酸为6.0g.通过计算,判断该药片中氢氧化铝的含量是否达到标准以及该药片中氢氧化铝的质量分数.
人的胃酸过多,会引起胃病.如图所示是某抗酸药标签上的部分文字.某同学为了测定该药中氢氧化铝的质量分数,进行如下操作:取一片药片(药片质量0.5g),研碎后加20mL蒸馏水,然后用质量分数为5%的盐酸至反应完全(其他成分不与盐酸反应),测定实验中反应掉的盐酸为6.0g.通过计算,判断该药片中氢氧化铝的含量是否达到标准以及该药片中氢氧化铝的质量分数.