题目内容
17. 某同学家中有一袋化肥,如图是氮肥包装标签的部分文字
某同学家中有一袋化肥,如图是氮肥包装标签的部分文字求:(1)此化肥100千克中氮元素的质量?
(2)此化肥中硫酸铵的质量分数(纯度)?
分析 (1)由题意,此硫酸铵化肥的含氮量为20%,据此进行分析解答.
(2)混合物中某化合物的质量分数(纯度)=$\frac{含杂质物质元素的质量分数}{物质中某元素的质量分数}$×100%,进行分析解答.
解答 解:(1)此硫酸铵化肥的含氮量为20%,此化肥100千克中氮元素的质量为100kg×20%=20kg.
(2)硫酸铵中氮元素的质量分数为$\frac{14×2}{(14+1×4)×2+32+16×4}×$100%≈21.2%.
此化肥中硫酸铵的质量分数为$\frac{20%}{21.2%}×$100%≈94.3%.
答:(1)此化肥100千克中氮元素的质量为20kg;(2)此化肥中硫酸铵的质量分数为94.3%.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
相关题目
12.t1℃时,分别将20g甲、乙两种晶体(不含结晶水)加入盛有100g水的两个烧杯中,恰好完全溶解,升温到t2℃时出现甲、乙烧杯中所示图1的现象.根据上述实验,结合如图2中甲、乙两物质的溶解度曲线,判断下列说法不正确的是(改编)( )


| A. | t1℃时烧杯中甲、乙两物质形成的溶液是饱和溶液 | |
| B. | t1℃时烧杯中甲的溶液溶质质量分数约为16.7% | |
| C. | t2℃时烧杯中甲物质溶液的质量是115g | |
| D. | 甲物质可能是氢氧化钙 |
6.某同学在用高锰酸钾加热制氧气时,若出现试管炸裂现象,其原因不可能是( )
| A. | 加热前试管外壁有水 | B. | 试管夹夹在试管的中上部 | ||
| C. | 试管口略向上倾斜了 | D. | 加热不均匀,局部温度过高 |
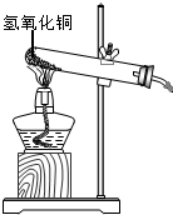 氢氧化铜固体受热分解能得到两种产物,其中一种为固体,某兴趣小组为确定这种固体产物,进行了如下探究活动.
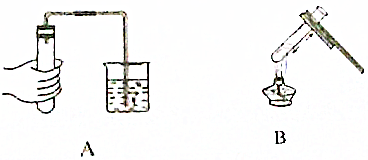
氢氧化铜固体受热分解能得到两种产物,其中一种为固体,某兴趣小组为确定这种固体产物,进行了如下探究活动. 为测定空气的成分,某学生设计了如图所示的实验装置.
为测定空气的成分,某学生设计了如图所示的实验装置. 如图是某化肥包装标签上的部分文字,请根据相关的信息计算:
如图是某化肥包装标签上的部分文字,请根据相关的信息计算: