题目内容
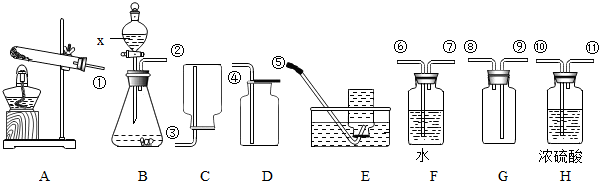
20.根据如图所示的实验回答问题: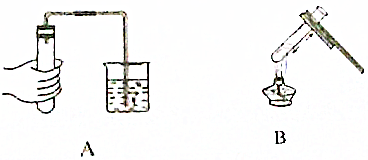
(1)实验A的名称是检查装置的气密性;
(2)实验A的原理是温度升高,气压增大;
(3)实验B中液体的体积不能超过试管容积的$\frac{1}{3}$;
(4)实验B中哪些错误的操作会导致试管破裂(写出一点)用焰心加热或试管外壁有水等.
分析 根据检验装置的气密性的方法是:先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出,以及给试管加热的正确操作进行分析.
解答 解:(1)通过分析可知,实验A的名称是:检查装置的气密性;
(2)实验A的原理是:温度升高,气压增大;
(3)实验B中液体的体积不能超过试管容积的$\frac{1}{3}$;
(4)玻璃是热的不良导体,受热不均会使试管炸裂,所以会导致试管破裂的操作有:用焰心加热或试管外壁有水等.
故答案为:(1)检查装置的气密性;
(2)温度升高,气压增大;
(3)$\frac{1}{3}$;
(4)用焰心加热或试管外壁有水等.
点评 本考点考查了检查装置的气密性、配制溶液、气体的除杂和收集等,要加强记忆有关的知识点,并理解记忆.本考点主要出现在选择题和填空题中.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目
8.许多在水溶液的反应(如复分解反应),往往有易溶物转化为难溶物或难溶物转化为更难溶物的现象.下表为相同温度下某些物质的溶解度:
(1)若在含有氯化银固体的水中加入硫化钠溶液,可能发生的现象是AgCl白色固体表面变黑.
(2)生产硫酸铵化肥的方法之一是:把石膏(CaSO4•2H2O)粉悬浮于水中,不断通入氨气再通入二氧化碳,充分反应后,立即过滤,滤液经蒸发而得到硫酸铵晶体.该反应的化学方程式为CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH 4)2SO4.
| 物质 | AgCl (白色) | Ag2S (黑色) | CaSO4 (白色) | Ca(OH)2 (白色) | Ca(HCO3)2 (白色) | CaCO3 (白色) | NH4HCO3 无色透明 | (NH4)2SO4 无色透明 |
| 溶解 度/g | 1.5×10-4 | 1.3×10-6 | 0.2 | 0.165 | 16.6 | 0.0015 | 21 | 75.4 |
(2)生产硫酸铵化肥的方法之一是:把石膏(CaSO4•2H2O)粉悬浮于水中,不断通入氨气再通入二氧化碳,充分反应后,立即过滤,滤液经蒸发而得到硫酸铵晶体.该反应的化学方程式为CaSO4+2NH3+CO2+H2O=CaCO3↓+(NH 4)2SO4.
5.下列图示的实验操作错误的是( )
| A. |  稀释浓硫酸 | B. |  倾倒液体 | C. |  检查气密性 | D. |  测定溶液pH 测定溶液pH |
12.如图所示的四个装置图及其使用方法的说明中,错误的一项是( )
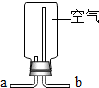 | 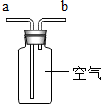 | 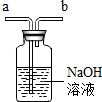 | 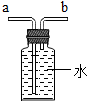 |
| 用排空气法收集CO2,则CO2从b管通入 | 用排空气法收集O2,则O2从a管通入 | 除去空气中的CO2,则空气从a管通入 | 用排水法收集O2,则O2从b管通入 |
| A. | A | B. | B | C. | C | D. | D |
9. 在实验室中用MnO2做为KClO3分解制氧气的催化剂,化学方程式为:
在实验室中用MnO2做为KClO3分解制氧气的催化剂,化学方程式为:
2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
小明想知道CuO、Fe2O3等氧化物是否也能对KClO3的分解起催化作用,且它们的催化能力是否相同.于是在实验室进行相关实验,获得实验数据如下表:
(1)该探究实验的自变量为催化剂的种类.
(2)结合实验数据分析,小明如何能知道各种催化剂的催化能力强弱?看该实验中产生等质量的氧气,所消耗的时间越长,催化剂的催化能力越弱.
(3)设置第1组实验的目的为对照,凸显氧化铁、氧化铜等物质对双氧水分解有催化能力.
 在实验室中用MnO2做为KClO3分解制氧气的催化剂,化学方程式为:
在实验室中用MnO2做为KClO3分解制氧气的催化剂,化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑
小明想知道CuO、Fe2O3等氧化物是否也能对KClO3的分解起催化作用,且它们的催化能力是否相同.于是在实验室进行相关实验,获得实验数据如下表:
| 实验 组别 | KClO3质量(克) | 催化剂 | 产生气体 质量(克) | 耗时 (秒) | |
| 化学式 | 质量(克) | ||||
| 1 | 0.60 | - | - | 0.014 | 480 |
| 2 | 0.60 | MnO2 | 0.20 | 0.096 | 36.5 |
| 3 | 0.60 | CuO | 0.20 | 0.096 | 79.5 |
| 4 | 0.60 | Fe2O3 | 0.20 | 0.096 | 34.7 |
(2)结合实验数据分析,小明如何能知道各种催化剂的催化能力强弱?看该实验中产生等质量的氧气,所消耗的时间越长,催化剂的催化能力越弱.
(3)设置第1组实验的目的为对照,凸显氧化铁、氧化铜等物质对双氧水分解有催化能力.
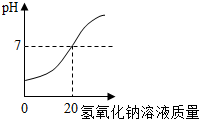 某科学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数.
某科学兴趣小组的同学在实验室配制质量分数为8%的氢氧化钠溶液,并用其测定某稀盐酸中溶质的质量分数. 某同学家中有一袋化肥,如图是氮肥包装标签的部分文字
某同学家中有一袋化肥,如图是氮肥包装标签的部分文字