题目内容
10.维生素C主要存在于蔬菜和水果中,其化学式是C6H8O6,维生素C的相对分子质量为176,维生素C中碳、氢、氧元素的质量比为9:1:12,碳元素的质量分数为40.1%,4.4g维生素C中含氧元素2.4g.分析 根据相对分子质量为构成分子的各原子的相对原子质量之和,化合物中各元素质量比=各原子的相对原子质量×原子个数之比,化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,化合物的质量=该化合物中某元素的质量÷该元素的质量分数,进行分析解答.
解答 解:维生素C的相对分子质量为6×12+8×1+6×16=176.
维生素C中碳、氢、氧三种元素的质量比为(12×6):(1×8):(16×6)=9:1:12.
碳元素的质量分数为$\frac{12×6}{176}×$100%≈40.1%.
需要维生素C的质量为2.4g÷($\frac{16×6}{176}×$100%)=4.4g.
故答案为:176;9:1:12;40.1%;4.4.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的有关计算进行分析问题、解决问题的能力.

练习册系列答案
 优加精卷系列答案
优加精卷系列答案
相关题目
18.小王从超市买回一些火腿肉,回家后尝了一下味道,觉得好像掺入了大量淀粉,可以证明是否掺入了淀粉的试剂是( )
| A. | 稀盐酸 | B. | 碘水或碘酒 | C. | pH试纸 | D. | 澄清的石灰水 |
5. 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
计算该样品中Na2CO3的质量分数.
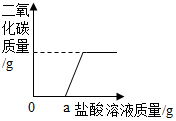
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(选填“大于”、“小于”或“等于”).
 一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.
一瓶久置的氢氧化钠固体已经发生了变质.某研究性学习小组为了探究变质程度,作出如下猜想:可能部分变质,固体是NaOH和 Na2CO3的混合物;可能全部变质,固体是Na2CO3.(1)首先对固体的成分进行确定.取少量固体于试管中,加水充分溶解,先加入足量的BaCl2 溶液,产生白色沉淀,静置后取上层清液,再加入CuSO4 溶液,产生蓝色絮状沉淀.根据实验现象,可确定该固体是NaOH和Na2CO3的混合物;
(2)称取10.6g 该固体样品于锥形瓶中,加入一定质量分数的稀盐酸,直至过量,得到数据如下表:
| 样品质量 | 反应前总质量 | 反应后总质量 |
| 10.6克 | 148.5克 | 146.3克 |
(3)再取固体样品溶于水,加入一定质量分数的稀盐酸,直至过量.测出加入稀盐酸的质量与产生CO2气体的质量关系如图所示.从图中可以判断:在该样品溶液中加入稀盐酸,首先与之反应的物质是NaOH.
(4)请你分析,一定质量的NaOH固体,变质前后与相同质量分数的稀盐酸反应,变质前消耗盐酸的量等于变质后消耗盐酸的量(选填“大于”、“小于”或“等于”).
15.某化合物完全燃烧,消耗9.6g氧气,生成8.8g二氧化碳和5.4g水,对该化合物的组成是( )
| A. | 含有C、H、O 三种元素 | B. | 只含有C、H 元素 | ||
| C. | 一定含有C、H可能含有O | D. | 无法确定 |
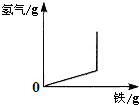
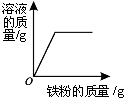
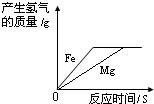
20.如图所示的四个图象,能正确反映对应变化关系的是( )
| A | B | C | D |
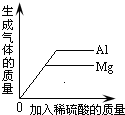
| 铁加入稀盐酸 | 向一定量的稀盐酸中加入铁粉 | 向两份体积和质量分数相同的盐酸中分别加入足量的铁粉和镁粉 | 向等质量的金属镁和铝中分别滴加足量且溶质质量分数相等的稀硫酸 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
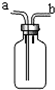 如图是化学中“著名”的多用途装置,有如下用途:
如图是化学中“著名”的多用途装置,有如下用途:


