题目内容
17.分离、除杂和检验是化学实验的重要环节,下面实验设计不能达到目的是( )| 实验内容 | 实验设计 | |
| A | 除去铜粉中少量的铁粉 | 加入足量的稀硫酸过滤 |
B | 提纯含有少量硝酸钾的氯化钠固体 | 先加入水溶解,蒸发到大量固体析出时,把剩余的少量液体倒掉,晾干即得到较纯净的氯化钠 |
| C | 验证某溶液为稀硫酸 | 先测溶液的pH<7,再加入锌粒有无色气体产生 |
| D | 分离二氧化碳和一氧化碳混合物 | 先用氢氧化钠溶液吸收掉二氧化碳分离出一氧化碳,再向该溶液中加足量稀硫酸“释放”出二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
分析 A、根据金属活动性顺序进行分析;
B、根据硝酸钾和氯化钠的溶解度受温度影响的关系进行分析;
C、根据溶液的pH<7,再加入锌粒有气泡冒出不一定是稀硫酸,还有可能是别的酸进行分析;
D、根据一氧化碳不和氢氧化钠溶液反应,而二氧化碳和氢氧化钠溶液反应生成碳酸钠和水,碳酸钠和稀硫酸反应生成硫酸钠、水和二氧化碳进行分析.
解答 解:A、混合物中加入稀硫酸,会与铁反应生成硫酸亚铁和氢气,然后剩下铜,故A正确;
B、硝酸钾的溶解度受温度影响较大,氯化钠的溶解度受温度影响较小,所以先加入水溶解,蒸发到大量固体析出时,把剩余的少量液体倒掉,晾干即得到较纯净的氯化钠,故B正确;
C、溶液的pH<7,再加入锌粒有气泡冒出不一定是稀硫酸,还有可能是别的酸,例如盐酸,故C错误;
D、一氧化碳不和氢氧化钠溶液反应,而二氧化碳和氢氧化钠钠溶液反应生成碳酸钠和水,碳酸钠和硫酸反应生成硫酸钠、水和二氧化碳,所以分离二氧化碳和一氧化碳混合物可用氢氧化钠溶液吸收掉二氧化碳分离出一氧化碳,再向该氢氧化钠溶液加足量稀硫酸“释放”出二氧化碳,故D正确.
故选:C.
点评 解答本题的关键是要充分理解各种物质的性质,只有这样才能对问题做出正确的判断,另外需要注意的就是选用的除杂试剂不能与原有物质反应,反应后不能引入新的杂质,还需要根据实际情况控制所选试剂的量.

练习册系列答案
相关题目
7.石墨需要通过化学变化才能体现出的性质是( )
| A. | 导电性 | B. | 质地较软 | C. | 可燃性 | D. | 黑色固体 |
5.观察能力是学好化学的重要因素之一,下列对实验现象的描述不正确的是( )
| A. | 将氢氧化钠溶液滴入紫色石蕊溶液中,氢氧化钠溶液变红色 | |
| B. | 细铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体,放出热量 | |
| C. | 铁锈放在足量盐酸中,铁锈逐渐变少,溶液逐渐变为黄色 | |
| D. | 硫酸铜固体溶于水可得到蓝色溶液 |
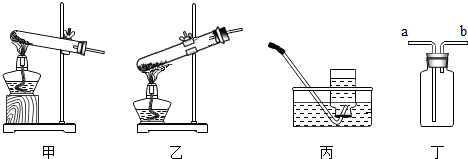
12.我们知道了二氧化锰可以作为过氧化氢制取氧气的催化剂,有部分同学为了探究二氧化锰是否对氯酸钾的分解起了催化作用,经查阅资料得知:氯酸钾的熔点为356℃,加热到400℃可观察到缓慢放出气泡,实验装置如图:
(1)实验设计如下,请你补充完成实验报告.
(2)以上实验中,该同学应选用装置甲来完成实验;
(3)写出第三步实验中发生的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)图“丙”中除导出气体外,另两个玻璃仪器的名称为水槽、集气瓶;若用装置“丁”收集氧气,则导出气体的导管口是b(填写编号“a”或“b”).

(1)实验设计如下,请你补充完成实验报告.
| 实验步骤 | 加热时间(min) | 实验现象 |
| ①将二氧化锰单独放入试管中加热,将带火星的木条放在试管口 | 10 | 木条无变化 |
| ②将氯酸钾单独放入试管中加热,将带火星的木条放在试管口 | 5 | 木条复燃 |
| ③将氯酸钾、二氧化锰混合放入试管中加热,带火星的木条放在试管口 | 1 | 木条复燃 |
(3)写出第三步实验中发生的化学方程式2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;
(4)图“丙”中除导出气体外,另两个玻璃仪器的名称为水槽、集气瓶;若用装置“丁”收集氧气,则导出气体的导管口是b(填写编号“a”或“b”).
2.影响空气质量的一组主要污染物是( )
| A. | NO2、N2和可吸入颗粒物 | B. | CO2、N2、O3 | ||
| C. | CO2、O2 和SO2 | D. | SO2、NO2和可吸入颗粒物(含PM2.5) |
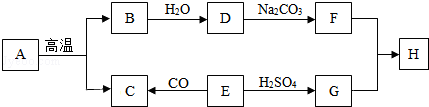
6.下列各组变化中,每一转化在一定条件下均能一步实现的是( )


| A. | ①② | B. | ②③ | C. | ①③ | D. | ①②③ |