题目内容
15.如图为元素周期表中某一周期元素的信息;请回答下列问题:
①表中磷原子的核电荷数x=15;
②表中其原子具有相对稳定结构的元素名称是氩;
③在化学反应中,每个铝原子失去3个电子形成铝离子;
④镁元素与氯元素形成的化合物化学式为MgCl2;
⑤第三周期第IVA的元素符号为Si.
分析 ①根据磷原子的结构示意图进行解答;
②根据元素的化学性质跟它的原子的最外层电子数目关系非常密切进行解答;
③根据铝原子最外层电子数为3,容易失去3个电子进行解答;
④根据化合物化学式的书写方法进行解答;
⑤周期数等于原子核外电子层数,族数等于最外层电子数.
解答 解:①根据磷原子的结构示意图可知,磷原子核外有15个电子,磷原子的核电荷数也为15;故答案为:15;
②元素的化学性质跟它的原子的最外层电子数目关系非常密切,当最外层电子数为8,则具有相对稳定结构,所以具有相对稳定结构的元素是氩元素;故答案为:氩;
③铝原子最外层电子数为3,容易失去3个电子;故答案为:3;
④根据化合物化学式的书写方法,镁元素容易失去2个电子显+2价,氯元素得到1个电子显-1价,镁元素与氯元素形成的化合物化学式为MgCl2;故答案为:MgCl2
⑤周期数等于原子核外电子层数,族数等于最外层电子数,所以第三周期第IVA的元素符号为Si.
故答案为:①15;②氩;③3;④MgCl2;⑤Si.
点评 本题考查学生根据原子结构示意图的特点,及提供的信息进行分析解题,并能灵活应用的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.某实验小组的同学为了测定实验室中高锰酸钾样品的质量分数,取7g该样品,依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
试计算:
(1)加热t3时间后高锰酸钾是否已经完全反应?是(填“是”或“否”);高锰酸钾中锰、氧元素的质量比为55:64.
(2)求完全反应后产生氧气的质量.
(3)求该样品中高锰酸钾的质量分数.(精确到0.1%)
| 加热时间 | t1 | t2 | t3 | t4 |
| 剩余固体质量/g | 6.88 | 6.55 | 6.36 | 6.36 |
(1)加热t3时间后高锰酸钾是否已经完全反应?是(填“是”或“否”);高锰酸钾中锰、氧元素的质量比为55:64.
(2)求完全反应后产生氧气的质量.
(3)求该样品中高锰酸钾的质量分数.(精确到0.1%)
3.下列有关化学实验的说法中不正确的是( )
| A. | 用高锰酸钾制02时,反应试管的管口应略向上倾斜 | |
| B. | 做铁在02中燃烧实验时,集气瓶应先放少量水或细沙 | |
| C. | 铁、锌、碘元素都属于微量元素 | |
| D. | 用金属和酸制H2时,可采用与制C02相同的发生装置 |
10.生活中发生的下列变化,属于化学变化的是( )
| A. | 活性炭吸附 | B. | 粮食酿酒 | ||
| C. | 汽油挥发 | D. | 分离液态空气制取氧气 |
20.在一个密闭容器内有X、Y、M、N四种物质,在一定条件下使它们发生化学反应,测得在反应一段时间前后各物质的质量如下:下列判断中正确的是( )
| 物质 | X | Y | M | N |
| 反应前质量(g) | 20 | 20 | 20 | 20 |
| 反应后质量(g) | 20 | 25 | 18 | 17 |
| A. | 密闭容器中发生的是分解反应 | B. | X一定是此反应中的催化剂 | ||
| C. | 此反应不遵守质量守恒定律 | D. | 参加反应的M与N的质量比为2:3 |
4. 研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
(1)取用二氧化锰的仪器是B(填编号).

(2)写出上述反应的文字表达式:过氧化$\stackrel{二氧化锰}{→}$氢水+氧气.
(3)实验3中,加入的二氧化锰质量应为5g.
(4)相同条件下,实验3产生氧气的速率最快,说明双氧水的浓度越大,反应速率越快.
【注意:若答对第(5)小题奖励4分,全卷总分不超过60分】
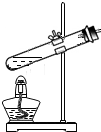
(5)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图中装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,请设计改进实验证明加热双氧水也可产生氧气:用排水法收集氧气并检验.
 研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间.
研究和控制化学反应条件有重要意义.同学们想探究双氧水的浓度对反应速率的影响.在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间. | 实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
| 1 | 10 | 40 | 5 | 200 |
| 2 | 20 | 30 | 5 | 100 |
| 3 | 30 | 20 | 5 | 67 |

(2)写出上述反应的文字表达式:过氧化$\stackrel{二氧化锰}{→}$氢水+氧气.
(3)实验3中,加入的二氧化锰质量应为5g.
(4)相同条件下,实验3产生氧气的速率最快,说明双氧水的浓度越大,反应速率越快.
【注意:若答对第(5)小题奖励4分,全卷总分不超过60分】
(5)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气.为了验证加热双氧水也可以产生氧气,同学们选择图中装置(气密性良好)进行实验.实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是氧气中混有较多的水蒸气,请设计改进实验证明加热双氧水也可产生氧气:用排水法收集氧气并检验.

