题目内容
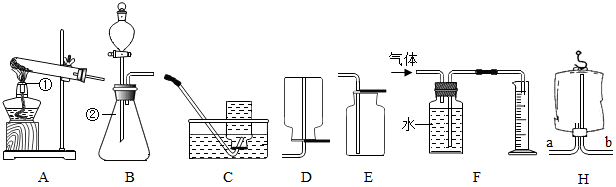
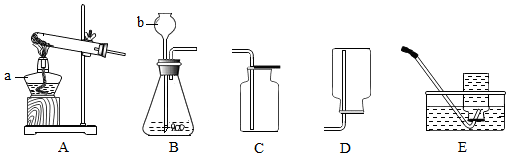
15.常温下,过氧化氢(H2O2)溶液在二氧化锰的催化作用下能迅速分解生成氧气和水.现有如图所示的实验装置(分液漏斗可以通过调节活塞控制液体的流速)现用5%过氧化氢溶液制取氧气,请回答有关问题.(1)写出标号仪器的名称:
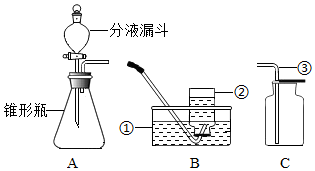
①锥形瓶②集气瓶③导管.
(2)分液漏斗中加入的物质是过氧化氢溶液,锥形瓶中加入的物质是二氧化锰.加入药品前要先检查装置的气密性.
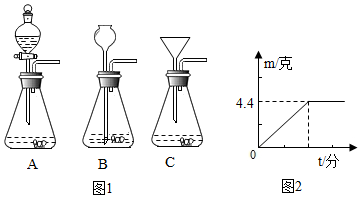
(3)写出该方法制取氧气的反应的文字表达式:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气.要收集一瓶较干燥的氧气,应选择收集装置C(填字母).
(4)若用此方法代替高锰酸钾制取氧气,其优点是B.(填字母)
A.生成物只有氧气 B.不需要加热C.需加热.
分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室用过氧化氢制取氧气时,分液漏斗中加入的物质是过氧化氢溶液,锥形瓶中加入的物质是二氧化锰,加入药品前要先检查装置的气密性进行分析;
(3)根据过氧化氢在二氧化锰的催化作用下分解生成水和氧气,向上排空气法收集的氧气干燥进行分析;
(4)根据过氧化氢制取氧气不需要加热,高锰酸钾制取氧气需要加热进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是锥形瓶,②是集气瓶,③是导管;
(2)实验室用过氧化氢制取氧气时,分液漏斗中加入的物质是过氧化氢溶液,锥形瓶中加入的物质是二氧化锰,加入药品前要先检查装置的气密性;
(3)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,文字表达式为:过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,向上排空气法收集的氧气干燥,所以要收集一瓶较干燥的氧气,应选择收集装置C;
(4)高锰酸钾制取氧气需要加热,操作复杂,过氧化氢制取氧气,不需要加热,操作简单,节省了能源,故选:B.
故答案为:(1)锥形瓶,集气瓶,导管;
(2)过氧化氢溶液,二氧化锰,气密性;
(3)过氧化氢$\stackrel{二氧化锰}{→}$水+氧气,C;
(4)B.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.

练习册系列答案
 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
20.燃烧与缓慢氧化的共同点是( )
| A. | 都需要氧气参与 | B. | 反应都很剧烈 | C. | 都是氧化反应 | D. | 都要点燃 |
7.铬(Cr)为不锈钢主要的添加元素,含量一般在12%以上.铬的表面生成一薄层致密的钝态氧化物保护膜是不锈钢具有耐蚀性主要原因.请回答下列问题:
(1)不锈钢是一种合金(填“合金”或“金属”).
(2)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
①上述三种金属的活动性由强到弱的顺序是Mg>Cr>Cu.
②从上述探究实验可知,Cr能(填“能”或“不能”)跟CuSO4溶液反应.若反应,请写出反应的化学方程式Cr+CuSO4=CrSO4+Cu.
(1)不锈钢是一种合金(填“合金”或“金属”).
(2)相同温度下,取大小相同、表面光亮的Cr、Mg、Cu三种金属薄片,分别投入等体积等溶质质量分数的足量稀盐酸中(反应中Cr显+2价),现象如下:
| 金属 | Cr | Mg | Cu |
| 与盐酸反应现象 | 放出气泡速率缓慢 | 放出气泡速率较快 | 无明显现象 |
②从上述探究实验可知,Cr能(填“能”或“不能”)跟CuSO4溶液反应.若反应,请写出反应的化学方程式Cr+CuSO4=CrSO4+Cu.
4.2015年6月1日,“东方之星”沉船事故救援时,潜水员钢瓶中携带的气体是( )
| A. | 水蒸气 | B. | 氮气 | C. | 氧气 | D. | 二氧化碳 |