题目内容
11.下列对物质的归类正确的是( )| 选 项 | 归 类 | 物 质 |
| A | 有机物 | 淀粉、油脂、酒精 |
| B | 挥发性酸 | 浓盐酸、浓硫酸、浓硝酸 |
| C | 可燃性气体 | 氢气、氧气、一氧化碳 |
| D | 形成酸雨的气体 | 二氧化硫、氮氧化物、二氧化碳 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据常见物质的性质、组成等分析判断有关的归类.
解答 解:A、淀粉、油脂、酒精都是含有碳元素的化合物,都属于有机物,故A正确;
B、浓盐酸、浓硝酸是具有挥发性的酸,浓硫酸是不具有挥发性的酸,故B错误;
C、氢气、一氧化碳是具有可燃性的气体,氧气不具有可燃性,具有助燃性,故C错误;
D、二氧化硫、氮氧化物是形成酸雨的气体,二氧化碳不是形成酸雨的气体,故D错误.
故选A.
点评 本题主要考查了常见物质的分类,熟悉常见物质的性质、组成等知识是解答本题的基础.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
1.下列制备物质的设计中,理论上正确的、操作上可行、经济上合理的是( )
| A. | CO$→_{△}^{CuO}$CO2$\stackrel{NaOH溶液}{→}$Na2CO3溶液 | |
| B. | Cu$\stackrel{AgNO_{3}溶液}{→}$Cu(NO3)2溶液$\stackrel{NaOH溶液}{→}$Cu(OH)2溶液 | |
| C. | Fe$→_{点燃}^{O_{2}}$Fe2O3$\stackrel{稀硫酸}{→}$Fe(S04)3溶液 | |
| D. | CaO$\stackrel{H_{2}O}{→}$Ca(OH)2溶液$\stackrel{Na_{2}CO_{3}溶液}{→}$NaOH 溶液 |
2.现有镁和硫酸镁固体混合物40克,平均分成4份,分别置于洁净的烧杯中,每个烧杯中先加入110.4克水,然后向烧杯中加入一定质量分数的稀硫酸,测得实验数据如表:
(1)计算实验中所用稀硫酸的溶质质量分数.
(2)计算恰好完成反应那次实验所得溶液中溶质的质量分数.
| 实验一 | 实验二 | 实验三 | 实验四 | |
| 原固体混合物的质量 | 10g | 10g | 10g | 10g |
| 加入稀硫酸的质量 | 20g | 40g | 80g | 85g |
| 生成气体的质量 | 0.1g | m | 0.4g | 0.4g |
(2)计算恰好完成反应那次实验所得溶液中溶质的质量分数.
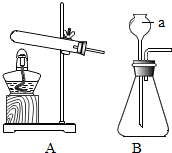
19.如图为实验室制取气体的常用装置.
(1)仪器a的名称是分液漏斗.
(2)用A装置作加热高锰酸钾制取氧气的发生装置,明显存在的不足是试管口没有棉花团,该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室制取二氧化碳应选择的发生装置是B.
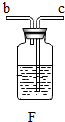
(4)实验室为得到干燥的O2,可将制得的气体从导管b通入装有浓硫酸溶液的F装置中,除去水蒸气.
| 发生装置 | 收集装置 | 洗气装置 |
 | 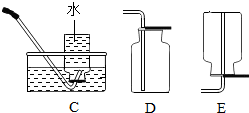 |  |
(2)用A装置作加热高锰酸钾制取氧气的发生装置,明显存在的不足是试管口没有棉花团,该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室制取二氧化碳应选择的发生装置是B.
(4)实验室为得到干燥的O2,可将制得的气体从导管b通入装有浓硫酸溶液的F装置中,除去水蒸气.
6.美国(自然)杂志报道,科学家在研究地下水时发现,处于地下深处两个矿物层中的水,由于受到高压的作用变成了类似“果冻”态的胶状体,呈仅几个分子厚度的水膜,黏度也大为增加,下列关于“果冻水”的说法中正确的是( )
| A. | 果冻水不属于氧化物 | B. | 果冻水中水分子不运动 | ||
| C. | 果冻水和普通水的化学性质相同 | D. | 果冻水与普通水物理性质相同 |
3.控制变量法是实验探究的重要方法,下列实验方法的设计中,能达到实验目的是( )


| A. | 图甲探究MnO2对H2O2分解的催化作用 | |
| B. | 图乙比较锌、铁的金属活动性强、弱 | |
| C. | 图丙探究可燃物的燃烧是否需要达到一定温度 | |
| D. | 图丁探究二氧化碳与水反应 |
1.下列离子能在pH=2的水溶液中大量共存的是( )
| A. | Cl-、NO3-、K+、Na+ | B. | HCO3-、Cl-、SO42-、Na+ | ||
| C. | SO42-、NO3-、K+、OH- | D. | NH4+、Cl-、OH-、K+ |
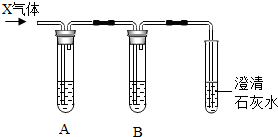 实验室用盐酸和碳酸钙固体反应,将得到的气体X通入澄淸的石灰水中,始终没有发现石灰水变浑浊,对此异常现象,同学们进行了如下探究活动:
实验室用盐酸和碳酸钙固体反应,将得到的气体X通入澄淸的石灰水中,始终没有发现石灰水变浑浊,对此异常现象,同学们进行了如下探究活动: