题目内容
19.请根据下列实验装置图回答问题: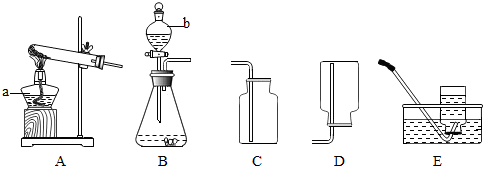
(1)写出仪器a、b的名称.
a是酒精灯;b是分液漏斗.
(2)用过氧化氢溶液制取氧气时,可选用的发生装置是B.化学方程式为反应中,二氧化锰起催化作用,加快了H2O2的分解.收集氧气可以采用C或E.
(3)甲烷是密度小于空气、难溶于水的气体,实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.制取甲烷的发生装置应选择A(填装置编号,下同),收集装置应选D或E;甲烷在空气中燃烧可生成二氧化碳和水.请写出甲烷完全燃烧的化学方程式CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(4)通过查阅资料得知,硫化氢是一种有毒的气体,其密度比空气的大,且能溶于水形成氢硫酸.实验室通常用块状固体硫化亚铁和稀硫酸混合,在常温下,通过发生反应制得硫化氢气体和硫酸亚铁.制取硫化氢气体得发生装置为A,收集装置为C.写出该反应的化学方程式为FeS+H2SO4═FeSO4+H2S↑;已知硫化氢气体在空气中燃烧可生成二氧化硫和水,请写出该反应的化学方程式2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O.
(5)氢气的密度小于空气且难溶于水,实验室可用固体锌和稀盐酸常温下反应制得氢气,同时生成硫酸锌;请写出该反应化学方程式为Zn+H2SO4═ZnSO4+H2↑;实验室制取并收集氢气的装置组合为BD或BE;写出氢气燃烧的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
分析 根据图示即可写出有关仪器的名称;气体的发生装置与反应物的状态和反应条件有关,收集方法与气体的密度和溶解性有关,根据化学方程式的书写方法书写化学方程式即可.
解答 解:(1)据图可以看出,a是酒精灯;b是分液漏斗,故填:酒精灯,分液漏斗.
(2)用过氧化氢溶液制取氧气时,是固液常温型反应,可选用的发生装置是B.化学方程式为反应中,二氧化锰起催化作用,加快了H2O2的分解.氧气的密度大于空气,不易溶于水,故收集氧气可以采用向上排空气法或是排水法,故填:B,催化,C,E.
(3)实验室用加热无水醋酸钠和碱石灰的固体混合物制取甲烷.是固体加热型反应,故制取甲烷的发生装置应选择A;由于甲烷是密度小于空气、难溶于水的气体,收集装置应选D或E;甲烷在空气中燃烧可生成二氧化碳和水,化学方程式为:CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.故填:A;D或E;CH4+2O2$\frac{\underline{\;点燃\;}}{\;}$CO2+2H2O.
(4)实验室通常用块状固体硫化亚铁和稀硫酸混合,在常温下,通过发生反应制得硫化氢气体和硫酸亚铁.是固液常温型反应,故制取硫化氢气体得发生装置为B,由于硫化氢是一种有毒的气体,其密度比空气的大,且能溶于水形成氢硫酸,故收集装置为C.硫化亚铁和稀硫酸反应生成硫酸亚铁和硫化氢,该反应的化学方程式为:FeS+H2SO4═FeSO4+H2S↑;硫化氢气体在空气中燃烧可生成二氧化硫和水,该反应的化学方程式为:2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O.故填:A;C;FeS+H2SO4═FeSO4+H2S↑;2H2S+3O2$\frac{\underline{\;点燃\;}}{\;}$2SO2+2H2O.
(5)实验室可用固体锌和稀盐酸常温下反应制得氢气,同时生成硫酸锌;该反应化学方程式为Zn+H2SO4═ZnSO4+H2↑;该反应是固液常温型反应,故发生装置为B,由于氢气的密度小于空气且难溶于水,故收集装置为D或E,故实验室制取并收集氢气的装置组合为BD或BE;氢气燃烧的化学方程式为2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O;故填:Zn+H2SO4═ZnSO4+H2↑;BD;BE;2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O.
点评 本题主要考查了实验室制取气体装置的选取,发生装置要看反应物的状态和反应条件,收集装置要看气体的密度和溶解性,并记住实验室制取氧气和二氧化碳的反应原理.

| 第1次 | 第2次 | 第3次 | 第4次 | |
| 加人稀硫酸质量/g | 50 | 50 | 50 | 50 |
| 剩余固体质量/g | 43.5 | 37.0 | 33.75 | 33.75 |
(2)当加入稀硫酸的质量为125g时,反应恰好完成.
(3)计算所用稀硫酸的浓度(写出计算过程).
查阅资料:CO2+Zn $\frac{\underline{\;\;△\;\;}}{\;}$CO+ZnO; FeCl3溶液遇KSCN溶液变红.
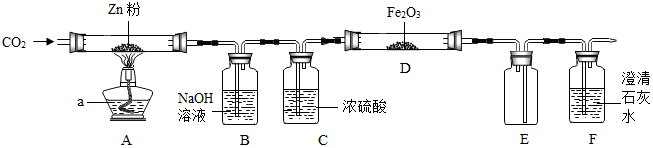
请回答下列问题:
(1)装置B的作用是吸收二氧化碳,发生的反应2NaOH+CO2═Na2CO3+H2O(化学方程式);某同学建议F后面应加一盏酒精灯,目的是把一氧化碳转化成二氧化碳.
(2)将研究小组分为两组,按如图装置进行对比实验:甲组用酒精灯、乙组用酒精喷灯对装置D进行加热,其产物均为黑色粉末(经检测为纯净物).两组分别用产物进行以下实验:
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入盐酸 | 溶解,无气泡,溶液呈浅黄绿色(含两种金属离子) | 溶解,有气泡,溶液呈浅绿色 |
| 2 | 取步骤1所得溶液,滴加KSCN溶液 | 变红 | 无现象 |
(3)通过该对比实验结果,你可以归纳出温度不同,一氧化碳还原氧化铁的生成物不同结论.
 研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧缺有明亮的火焰.该小组同学进行了如下探究:
研究小组在学习氧气的化学性质时发现:铁丝燃烧没有火焰,蜡烛燃烧缺有明亮的火焰.该小组同学进行了如下探究:①写出铁丝在氧气中燃烧的化学方程式:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4-
②探究一:蜡烛燃烧产生火焰的原因是什么?
点燃蜡烛,将金属导管一端伸入内焰,导出其中物质,在另一端管口点燃,也有火焰产生(如图).由此可知:蜡烛燃烧产生的火焰是由气态(填“固态”或“气态”)物质燃烧形成的.
③探究二:物质燃烧产生火焰的根本原因是什么?
查阅资料
| 物质 | 熔点╱℃ | 沸点╱℃ | 燃烧时温度╱℃ |
| 石蜡 | 50-70 | 300-550 | 约600 |
| 铁 | 1535 | 2750 | 约1800 |
| 钠 | 97.8 | 883 | 约1400 |
④木炭在氧气中燃烧没有火焰,其原因可能是燃烧时的温度低于沸点.
 如图所示为过滤的操作实验,请按要求回答下列问题:
如图所示为过滤的操作实验,请按要求回答下列问题: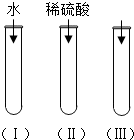 氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动
氧化铜(CuO)是一种黑色固体,可溶于稀硫酸中.某同学想知道是稀硫酸中的H2O、H+和SO42-中的哪种粒子能使氧化铜溶解.请你和他一起通过如图所示三个实验来完成这次探究活动