题目内容
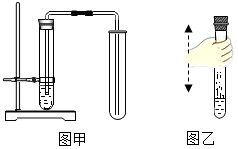
11.某化学兴趣小组查阅资料得知:过氧化钠(Na2O2)是一种黄色粉末,常温下能与二氧化碳反应产生氧气,常用在潜水艇中作供氧剂.该小组同学将过氧化钠与二氧化碳反应后,发现除了生成氧气,还生成了一种白色固体.【提出问题】该白色固体是什么?
【猜想】猜想a:碳酸钠(Na2CO3 ) 猜想b:碳酸氢钠(NaHCO3)
小周同学认为猜想b不成立,理由是反应物中没有氢(H) 元素.
【实验】取少量生成的白色固体于试管中,加入稀盐酸(稀HCl),产生气泡,再将生成的气体通入澄清石灰水中,石灰水变浑浊.
【结论】猜想a成立.
请写出过氧化钠与二氧化碳反应的化学方程式2Na2O2+2CO2=2Na2CO3+O2.
【继续探究】过氧化钠能否与水反应?生成物是什么?
| 实验操作 | 实验现象 | 结论 |
| 1、取适量过氧化钠放入盛有水的烧杯中 | 固体溶解得无色溶液有能使带火星的木条复燃的气体生成. | 有氧气生成 |
| 2、向所得溶液中滴入硫酸铜溶液 | 有蓝色沉淀生成 | 过氧化钠能(填能否)与水反应 |
分析 【猜想】化学变化中元素的种类不变,反应物中不含氢元素,生成物中也不可能有氢元素;
【实验】要验证白色固体是Na2CO3,只要证明含有CO32-离子就可以,其方法是:滴加稀盐酸,产生能使澄清石灰水变浑浊的气体;
【结论】根据反应物、生成物以及反应条件正确书写化学反应方程式;
【继续探究】1、由实验结论“过氧化钠能与水反应生成氧气”推知,氧气能使带火星的木条复燃;
2、根据酚酞试液的性质以及实验结论“所得溶液呈碱性”进行填空.
解释与结论:根据实验中验证的过氧化钠的性质进行填空.
解答 解:【猜想】因为反应物过氧化钠(Na2O2)和二氧化碳(CO2)中均无氢(H)元素,所以生成物中不可能有含有氢(H)元素的碳酸氢钠(NaHCO3);
故答案是:氢(H);
【实验】检验碳酸钠,只要验证有碳酸根离子即可,其验证方法为:取少量白色固体于试管中,加入稀盐酸,看到有气泡产生,将生成气体通入澄清石灰水,看到澄清石灰水变浑浊,则证明是Na2CO3;
故答案是:稀盐酸(稀HCl);
【结论】由以上实验现象可以推知,过氧化钠与二氧化碳在常温下发生反应生成碳酸钠和氧气,其反应方程式为:2Na2O2+2CO2=2Na2CO3+O2;
故答案是:2Na2O2+2CO2=2Na2CO3+O2;
【继续探究】①根据实验结论知,过氧化钠能与水反应生成氧气,而氧气能使带火星的木条复燃;
故答案是:氧气;
②向所得溶液中滴入硫酸铜溶液,会观察到有蓝色沉淀生成,说明生成氢氧化铜蓝色沉淀,则“所得溶液呈碱性”,所以该生成物中含有氢氧化钠,即过氧化钠 能(填能否)与水反应.
故答案是:能;
解释与结论:过氧化钠能与水反应生成氧气和一种碱,则可写出此反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑
故答案是:2Na2O2+2H2O=4NaOH+O2↑.
点评 该题根据查阅资料提供的信息并结合实验步骤和现象解决问题.主要考查读题能力,能把题目所给信息与所学知识进行牵连.知道性质决定用途,用途体现性质.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 铜丝做导线 | B. | 石墨做铅笔芯 | C. | 铁做锅 | D. | 酒精做燃料 |
| 物质 | 选用的试剂和方法 | |
| A | 空气、氧气和氮气 | 燃着的木条 |
| B | 硬水和软水 | 肥皂水 |
| C | 盐酸溶液和硫酸溶液 | 碳酸钠溶液 |
| D | 棉纤维和羊毛纤维 | 抽丝灼烧 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 分别溶于水 | B. | 用燃着的木条实验 | ||
| C. | 比较轻重 | D. | 将它们分别通入澄清石灰水 |
| A. | 催化剂在化学反应里只是加快化学反应速率 | |
| B. | 化合反应不一定是氧化反应,氧化反应一定是化合反应 | |
| C. | 为了减少空气污染,应禁止使用煤等化石燃料,开发使用太阳能等新能源 | |
| D. | 给物质加热时,试管外壁要擦干,目的是防止试管炸裂 |