题目内容
18.从水分子分解示意图中我们能获得许多信息,其中描述正确的是( )
| A. | 这是一个化合反应 | |
| B. | 在化学变化中氢原子和氧原子是最小的粒子 | |
| C. | 水是由氢气和氧气组成的 | |
| D. | 在化学变化中氢分子和氧分子都没有发生变化 |
分析 A、根据反应的特点对反应的类型进行判断;
B、根据微粒的变化分析分子原子的变化等;
C、根据微粒的构成分析物质的组成;
D、根据微粒的变化分析分子原子的变化等.
解答 解:A、由水分子分解示意图可知,该反应由一种物质反应后生成两种物质的反应,为分解反应而不是化合反应,故A不正确;
B、由微粒的变化可知,在化学变化中氢原子和氧原子没有变化,是化学变化中的最小的粒子,故B正确;
C、由微粒的构成可知,水是由氢元素和氧元素组成的,故C不正确;
D、由微粒的变化可知,在化学变化中氢原子和氧原子都没有发生变化,氢分子和氧分子是生成物,故D不正确.
故选B.
点评 变化的微观示意图,可以直观地反映出变化发生的过程,根据对变化过程中各物质构成的对比与分析,可判断化学变化的实质:分子变成原子,原子重新结合成新的分子.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列氯元素的物质中,氯元素化合价由低到高排列的一组是( )
| A. | NaCl Ca(ClO)2 KClO3 | B. | Cl2 HCl ClO2 | ||
| C. | KClO3 NaClO2 HClO4 | D. | NH4ClO4 Cl2O3 HClO3 |
3.某制碱厂以海水为主要原料生产纯碱(碳酸钠)和其他副产品.
I.将海水进行处理后获得精盐水.海水中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质.将杂质转化为沉淀过滤除去,在向滤液中加入适量的盐酸得到精盐水,该工艺示意如图1:

(1)对该过程的认识中,不正确的是AC
A.操作①中需要进行搅拌,目的是提高氯化钠的溶解度
B.操作③、④两步顺序可以颠倒
C.操作⑤得到的沉淀中有三种成分的物质
D.操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
(2)加入碳酸钠溶液的目的是除去氯化钙和过量的氯化钡.
II.将精盐水制成饱和溶液,先向其中通入足量的氨气,在向其中通入足量的二氧化碳至有大量晶体(碳酸氢钠,NaHCO3)析出,反应的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓:将晶体转移出来后,加热至不在有气体产生,所得固体即为纯碱.
(3)加热晶体碳酸氢钠获得纯碱的化学方程式为2NaHCO$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(4)制碱过程中获得的副产品可做化肥,其化学式为NH4Cl.
组成确定
(5)①称取一定质量的纯碱样品,经多次充分加热后,在称重,质量无变化:②另取少量纯碱样品加入适量水,样品完全溶液,向该溶液中加入过量稀HNO3,在滴加AgNO3溶液,有白色沉淀.由上述实验可确定纯碱样品含有杂质NaCl(化学式).
含量确定
(6)称取纯碱样品21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图2所示.请通过计算并结合下表判断此纯碱样品等级为合格品.
总结反思
(7)某同学认为,在上述纯碱含量测定过程中,如果测得结果比实际纯度高,可能原因是稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大.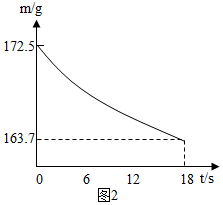
I.将海水进行处理后获得精盐水.海水中,除氯化钠外,还含有氯化镁、氯化钙、硫酸钠等杂质.将杂质转化为沉淀过滤除去,在向滤液中加入适量的盐酸得到精盐水,该工艺示意如图1:

(1)对该过程的认识中,不正确的是AC
A.操作①中需要进行搅拌,目的是提高氯化钠的溶解度
B.操作③、④两步顺序可以颠倒
C.操作⑤得到的沉淀中有三种成分的物质
D.操作⑥中,加入盐酸的目的是除去过量的氢氧化钠和碳酸钠,将滤液的pH调为7
(2)加入碳酸钠溶液的目的是除去氯化钙和过量的氯化钡.
II.将精盐水制成饱和溶液,先向其中通入足量的氨气,在向其中通入足量的二氧化碳至有大量晶体(碳酸氢钠,NaHCO3)析出,反应的化学方程式为:NaCl+NH3+CO2+H2O=NH4Cl+NaHCO3↓:将晶体转移出来后,加热至不在有气体产生,所得固体即为纯碱.
(3)加热晶体碳酸氢钠获得纯碱的化学方程式为2NaHCO$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O.
(4)制碱过程中获得的副产品可做化肥,其化学式为NH4Cl.
组成确定
(5)①称取一定质量的纯碱样品,经多次充分加热后,在称重,质量无变化:②另取少量纯碱样品加入适量水,样品完全溶液,向该溶液中加入过量稀HNO3,在滴加AgNO3溶液,有白色沉淀.由上述实验可确定纯碱样品含有杂质NaCl(化学式).
含量确定
(6)称取纯碱样品21.5g,加入到盛有足量稀盐酸的烧杯中,并不断用玻璃棒搅拌.反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图2所示.请通过计算并结合下表判断此纯碱样品等级为合格品.
| 工业纯碱标准:(Na2CO3%≥) | ||
| 优等品 | 一等品 | 合格品 |
| 99.2 | 98.8 | 98.0 |
(7)某同学认为,在上述纯碱含量测定过程中,如果测得结果比实际纯度高,可能原因是稀盐酸挥发出的HCl气体随CO2气体排出,从而导致所测纯度偏大.

10.高铁酸钾(K2FeO4)是一种集吸附、凝聚、杀菌等功能为一体的新型高效水处理剂.下列说法不正确的是( )
| A. | K2FeO4是一种纯净物 | |
| B. | K2FeO4由三种元素组成 | |
| C. | K2FeO4中钾、铁、氧三种元素的质量比是2:1:4 | |
| D. | K2FeO4的相对分子质量是198 |
2.下列图示实验操作中,正确的是( )
| A. |  | B. |  | C. |  | D. |  |

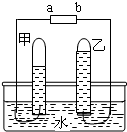 如图是电解水的简易装置.
如图是电解水的简易装置.