题目内容
18.金属材料与人类的生产和生活息息相关.(1)金属材料包括纯金属和它们的合金.人们大量使用的是合金而不是纯金属,这是因为合金具有更多优良性能,例如钢比纯铁硬度大(填“大”或“小”).
(2)使用铜制作电线,是利用了铜的导电性.
(3)小明发现家里的铁炒锅生锈了,为了防止铁锅生锈,你给他的建议是保持铁锅表面的洁净干燥.
(4)将带锈铁钉放入试管,加入过量稀盐酸,看到铁锈消失,溶液呈黄色,反应的化学方程式为Fe2O3+6HCl═2FeCl3+3H2O,待铁锈消失后又看到的现象为有气泡冒出.
分析 根据已有的金属的性质进行分析解答,金属材料包括纯金属和合金,铜具有良好的导电性,根据防锈的方法解答,氧化铁和铁都能与盐酸反应,据此解答.
解答 解:(1)金属材料包括纯金属和它们的合金,钢的硬度大于纯铁,故填:合金,大;
(2)使用铜制作电线,是利用了铜的导电性,故填:导电性;
(3)为了防止铁锅生锈,可以在铁锅使用后洗净擦干,故填:保持铁锅表面的洁净干燥;
(4)氧化铁与盐酸反应生成氯化铁和水,铁锈消失后铁与盐酸反应生成氢气,会观察到有气泡产生,故填:Fe2O3+6HCl═2FeCl3+3H2O,有气泡冒出.
点评 本题考查的是金属材料的有关应用的知识,完成此题,可以依据已有的金属的性质进行.

练习册系列答案
相关题目
8.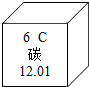 如图是元素周期表中碳元素的相关信息,下列说法错误的是( )
如图是元素周期表中碳元素的相关信息,下列说法错误的是( )
 如图是元素周期表中碳元素的相关信息,下列说法错误的是( )
如图是元素周期表中碳元素的相关信息,下列说法错误的是( )| A. | 碳的相对原子质量为12.01 | |
| B. | 碳元素位于元素周期表的第二周期 | |
| C. | 碳元素是形成化合物种类最多的元素 | |
| D. | 含有碳元素的物质都具有可燃性 |
9.两种金属混合物30g,投入足量盐酸中,产生1g氢气,则组成该混合物的不可能是( )
| A. | Fe、Zn | B. | Al、Zn | C. | Mg、Al | D. | Mg、Cu |
13. 甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )
 甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )
甲、乙两种物质的溶解度曲线如图所示,下列叙述正确的是( )| A. | t1℃时甲和乙的饱和溶液,升温到t2℃时仍是饱和溶液 | |
| B. | t1℃时,甲和乙的溶解度相等 | |
| C. | 当温度高于0℃而低于t1℃时,甲的溶解度比乙的溶解度大 | |
| D. | t2℃时,甲、乙的饱和溶液各100g,其溶质的质量一定相等 |
3.将镁条放入盛有硫酸铜溶液的试管中,可以观察到镁条表面析出紫红色固体的同时有气泡产生,用点燃的火柴试验该气体,能产生微弱的淡蓝色火焰,同时可听到轻微的爆鸣声.小黄同学就该实验现象的一些推论正确的是( )
| A. | 硫酸铜溶液在物质分类上属于化合物中的盐类 | |
| B. | 由轻微的爆鸣声可知有氢气生产,说明该硫酸铜溶液中一定混入某种酸溶液 | |
| C. | 用点燃的火柴试验,能产生微弱的淡蓝色火焰,说明该气体的主要性质是还原性 | |
| D. | 镁条放入硫酸铜溶液中有气泡产生,可以大胆推测硫酸铜溶液可能呈酸性 |
8.下列实验操作不正确的是( )
| A. |  检查气密性 | B. |  氢气验纯 | C. |  检验氧气 | D. |  二氧化碳验满 |
