题目内容
14. 实验室用H2还原CuO得到红色固体Cu,但其中是否含有Cu2O(红色),某研究性学习小组进行了认真的探究
实验室用H2还原CuO得到红色固体Cu,但其中是否含有Cu2O(红色),某研究性学习小组进行了认真的探究【查阅资料】
①无水CuSO4遇水变蓝;
②高温灼烧Cu首先会生成CuO,CuO继续生成Cu2O和O2;
③Cu2O和空气中的成分在高温和常温下均不反应
④Cu2O与稀H2SO4反应:Cu2O+H2SO4═Cu+CuSO4+H2O
【设计实验方案】
方案1:将该红色固体加入稀H2SO4中,若现象为部分固体溶解,溶液由无色变成蓝色,则红色固体中含有Cu2O.
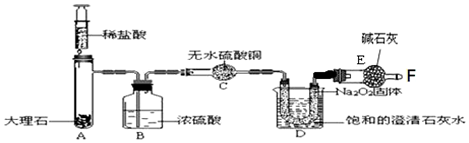
方案2:装置如图所示,将红色固体装入硬质玻璃管,拟通过干燥管中CuSO4变蓝来判断红色固体是否含有Cu2O,为确保探究的科学、合理、安全,实验中还应采取的措施有①②④(填序号)
①加热前先排尽装置中的空气②在氢气发生器与硬质玻璃管之间加一个干燥装置
③在硬质玻璃管和无水硫酸铜干燥管之间加一个干燥装置;
④在盛有无水硫酸铜的干燥管后再连接一个装有浓硫酸的洗气瓶.
方案3:取一定质量为a克的干燥坩埚,将红色固体置于坩埚中称得总质量为b克,在空气中高温灼烧至质量恒定,称量最后坩埚与固体总质量为c克,若确认红色固体中含有Cu2O,则c与a,b应符合的数字关系式为c+0.25a<1.25b.
分析 氧化亚铜和稀硫酸反应生成硫酸铜、铜和水,硫酸铜溶液是蓝色溶液;
氢气是可燃性气体,和空气或氧气混合达到一定程度时遇明火会发生爆炸;
加热条件下,铜能和空气中的氧气反应生成氧化铜.
解答 解:方案1:
铜不能和稀硫酸反应,将该红色固体加入稀H2SO4中,若部分固体溶解,溶液由无色变成蓝色,则红色固体中含有Cu2O.
故填:部分固体溶解,溶液由无色变成蓝色.
方案2:
①加热前先排尽装置中的空气,以免发生爆炸,从而确保安全;
②在氢气发生器与硬质玻璃管之间加一个干燥装置,以除去氢气中的水蒸气,以免影响对生成物水的检验;
③在硬质玻璃管和无水硫酸铜干燥管之间加一个干燥装置时,会影响对生成物水的检验;
④在盛有无水硫酸铜的干燥管后再连接一个装有浓硫酸的洗气瓶,以免空气中的水蒸气影响实验结果;
因此为确保探究的科学、合理、安全,实验中还应采取的措施有①②④.
故填:①②④.
方案3:
假设红色固体全部是铜,设反应生成氧化铜质量为x,
2Cu+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuO,
128 160
(b-a)g x
$\frac{128}{(b-a)g}$=$\frac{160}{x}$,
x=1.25(b-a)g,
若确认红色固体中含有Cu2O,则(c-a)g<1.25(b-a)g,即c与a,b应符合的数字关系式是c+0.25a<1.25b,
故填:c+0.25a<1.25b.
点评 本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
相关题目
2.下列图象能正确反映所对应叙述关系的是( )
| A. |  向PH=3的溶液中不断加水 | |
| B. |  一定量的硫酸铜与锌粒反应 | |
| C. |  向H2SO4和CuSO4混合液中加NaOH溶液 | |
| D. | 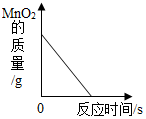 给氯酸钾和二氧化锰的混合物加热 |
9.“治污水”是“五水共治”行动中的一项,其实很多污水可以变废为宝,某电镀废水含有AgNO3和Zn(NO3)2,如果将洁净的铁丝进入该电镀废水中,一段时间后铁丝表面覆盖了一层物质,这层物质是( )
| A. | Ag、Zn | B. | Ag | C. | Zn | D. | Zn、Fe |
6.临床上发现,用25%的硫酸镁溶液l0~20mL与10%的葡萄糖溶液500mL的混合液可以治疗支气管哮喘.下表是硫酸镁的部分溶解度数据:
(1)若用无水硫酸镁固体配制400g 25%的硫酸镁溶液,则需要水的体积为300mL(假设此实验条件下水的密度为lg/mL),在配制溶液过程中玻璃棒的作用是搅拌,加快溶解速率.
(2)若要配制30%的硫酸镁溶液,则配制时应控制的溶液温度至少达到30℃.
| 温度(℃) | 10 | 20 | 30 | 40 | 60 | 80 |
| 溶解度(g/100g水) | 28.2 | 33.7 | 38.9 | 44.5 | 54.6 | 55.8 |
(2)若要配制30%的硫酸镁溶液,则配制时应控制的溶液温度至少达到30℃.
 盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中科学许多实验都用到了盐酸.
盐酸是一种重要的化工原料,也是实验室中重要的化学试剂,初中科学许多实验都用到了盐酸.