题目内容
15.人类生存需要清新的空气,下列情况不会造成空气污染的是( )| A. | 使用太阳能热水器 | B. | 燃放烟花 | ||
| C. | 光合作用 | D. | 汽车尾气 |
分析 本题主要是空气的污染及其危害,空气污染的途径主要有两个:有害气体和粉尘.有害气体主要有一氧化碳、二氧化硫、二氧化氮等气体;粉尘主要指一些固体小颗粒.
解答 解:A、使用太阳能热水器,不会造成空气污染,故选项正确;
B、燃放烟花生成有害气体和烟尘,会污染空气,故选项错误;
C、光合作用生成氧气,不会造成空气污染,故选项正确;
D、汽车尾气有一氧化碳、一氧化氮等气体,污染空气,故选项错误;
故选A C;
点评 本考点考查了空气的污染及其危害,环保问题已经引起了全球的重视,本考点的基础性比较强,主要出现在选择题和填空题中.

练习册系列答案
相关题目
5. 化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.
化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.
【提出问题】导致溶液pH变化的原因是什么?
【查阅资料】(1)溶液的pH是由H+或OH-浓度决定,H+浓度越大,
pH越小;OH-浓度越大,pH越大.
(2)溶液中某种离子浓度非常小时,可忽略不计.
【作出猜想】猜想①:溶液pH变化是因为氢氧化钠溶液被稀释.
猜想②:溶液pH变化是因为发生了化学反应.
【进行实验】同学们分成两组分别进行实验.
甲组:同学们将4mL2%的稀硫酸换成4mL水,逐滴滴加到2mL2%的氢氧化钠溶液中,并测得溶液的pH始终大于7,说明猜想Ⅰ不合理.
乙组:同学们分别取a、b、c三处溶液进行实验.
【实验结论】猜想Ⅱ合理.
【知识拓展】从微观角度分析,中和反应的实质是H+和OH-反应变成H2O.
 化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.
化学兴趣小组同学进行中和反应实验时,将4mL2%的稀硫酸逐滴滴加到2mL2%的氢氧化钠溶液中,测得溶液的pH变化曲线如图所示.【提出问题】导致溶液pH变化的原因是什么?
【查阅资料】(1)溶液的pH是由H+或OH-浓度决定,H+浓度越大,
pH越小;OH-浓度越大,pH越大.
(2)溶液中某种离子浓度非常小时,可忽略不计.
【作出猜想】猜想①:溶液pH变化是因为氢氧化钠溶液被稀释.
猜想②:溶液pH变化是因为发生了化学反应.
【进行实验】同学们分成两组分别进行实验.
甲组:同学们将4mL2%的稀硫酸换成4mL水,逐滴滴加到2mL2%的氢氧化钠溶液中,并测得溶液的pH始终大于7,说明猜想Ⅰ不合理.
乙组:同学们分别取a、b、c三处溶液进行实验.
| 实验操作 | 实验现象 | 实验分析 |
| 取适量a处溶液于试管中,加入镁条 | 无气泡产生 | 溶液中几乎不含H+(填离子符号) |
| 取适量b处溶液于试管中,加入紫色石蕊溶液 | 石蕊溶液不变色 | 溶液中几乎不含H+和OH- |
| 取适量c处溶液于试管中,加入硫酸铜溶液 | 无沉淀产生 | 溶液中几乎不含OH- |
【知识拓展】从微观角度分析,中和反应的实质是H+和OH-反应变成H2O.
10.某课外兴趣小组的同学为了探究金属X、Y、Z三种金属的活动性顺序,进行实验进行了如下探究,请你加入他们一起完成探究:
实验一:把金属X、Y、Z三种金属分别放入硫酸溶液中
(1)Z与硫酸反应后,生成+3价金属离子,写出实验③的化学方程式2Z+3H2SO4═Z2(SO4)3+3H2↑(金属就用Z表示);
实验二:为了比较X、Y两种金属的活动性,把X、Y两种金属丝放入硝酸银溶液中.
(2)通过实验二并结合实验一的现象分析,可得出X、Y、Z金属活动性由强到弱的顺序为:Z>X>Y.
实验三:同学们接着对“Z丝和硫酸反应的快慢与什么因素有关”的课题开展探究,下表是他们分别用相同质量的Z丝和足量稀硫酸反应的三组实验数据:
(3)实验⑦和⑧表明:该反应快慢与温度有关;
(4)能表明硫酸浓度对反应快慢有影响的实验编号是⑥⑦;
(5)如果实验⑥中硫酸的质量分数换为4%,请预测Z丝消失的时间(用t表示)的取值范围300s<t<500s.
(6)该实验除了用Z丝消失的时间来衡量反应的快慢的方法外,你还能提出的一种新的方法是比较收集相同体积气体需要的时间.
实验一:把金属X、Y、Z三种金属分别放入硫酸溶液中
| 实验序号 | ① | ② | ③ |
| 实验步骤 | 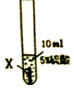 | 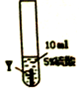 | 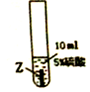 |
| 实验现象 | 在X片表面无明显变化 | Y片表面无明显变化 | Z片溶解,表面有无色氢气产生,溶液最终无色 |
实验二:为了比较X、Y两种金属的活动性,把X、Y两种金属丝放入硝酸银溶液中.
| 实验序号 | ④ | ⑤ |
| 实验步骤 | 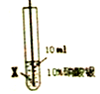 | 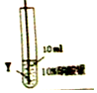 |
| 实验现象 | 在X丝表面有银白色的固体析出 | 在Y丝表面没有明显现象 |
实验三:同学们接着对“Z丝和硫酸反应的快慢与什么因素有关”的课题开展探究,下表是他们分别用相同质量的Z丝和足量稀硫酸反应的三组实验数据:
| 实验编号 | 硫酸的质量分数/% | 反应的温度 | Z丝消失的时间/S |
| ⑥ | 3 | 20 | 500 |
| ⑦ | 6 | 20 | 300 |
| ⑧ | 6 | 30 | 80 |
(4)能表明硫酸浓度对反应快慢有影响的实验编号是⑥⑦;
(5)如果实验⑥中硫酸的质量分数换为4%,请预测Z丝消失的时间(用t表示)的取值范围300s<t<500s.
(6)该实验除了用Z丝消失的时间来衡量反应的快慢的方法外,你还能提出的一种新的方法是比较收集相同体积气体需要的时间.
7.实验室许多药品需要密封保存.下列药品需要密封保存原因解释错误的是( )
| A. | 浓盐酸,防止挥发 | B. | NaOH固体,防止潮解和与CO2反应 | ||
| C. | 浓硫酸,防止吸水 | D. | 生石灰,防止与氧气反应 |
4.以美国为首的北约曾在科索沃战场上投下了至少10t的贫铀弹,使不少人患上了“巴尔干综合症”.贫铀弹的主要成分是低放射性的铀.这种铀原子的相对原子质量为238,质子数为92,则铀原子的核外电子数为( )
| A. | 238 | B. | 146 | C. | 136 | D. | 92 |
5.下列物质不属于酸的是( )
| A. | HNO3 | B. | NaHSO4 | C. | H2SO4 | D. | HCl |
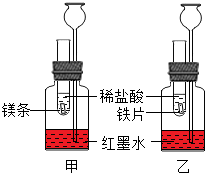 探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.
探究活动一:在室温条件下进行如图所示实验.已知:试管内的镁条和铁片表面均被打磨洁净,且形状、大小均相同;同时加入两支试管中的稀盐酸的质量和质量分数均相等.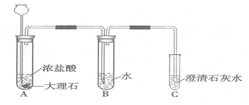 已知盐酸是HCl气体溶于水所形成的溶液.在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象.现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.回答下列问题:
已知盐酸是HCl气体溶于水所形成的溶液.在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象.现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.回答下列问题: