题目内容
8.下列关于葡萄糖(C6H12O6)的说法中,错误的是( )| A. | 属于有机物 | B. | 由三种元素组成 | ||
| C. | 每个分子中含有6个碳原子 | D. | 碳、氢、氧元素的质量比为1:2:1 |
分析 A.根据有机物与无机物的概念来分析;
B.根据物质的组成来分析;
C.根据分子结构来分析;
D.根据化合物中元素质量比的计算方法来分析.
解答 解:A.由葡萄糖的化学式C6H12O6可知,葡萄糖是一种含有碳元素的化合物,属于有机物,故正确;
B.由葡萄糖的化学式C6H12O6可知,葡萄糖含有C、H、O三种元素,故正确;
C.由葡萄糖的化学式C6H12O6可知,每个葡萄糖分子中含有6个碳原子,故正确;
D.葡萄糖中C、H、O元素的质量比是:(12×6):(1×12):(16×6)=6:1:8≠1:2:1,故错误.
故选D.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
18.质量分数不同的硫酸溶液其密度不相同,对照表如下:
(1)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是质量分数越大密度越大.
(2)质量分数80%和20%的两种硫酸溶液等体积混合后,溶液中溶质的质量分数是56.2%.(结果保留一位小数)
(3)欲配制300克溶质的质量分数为30%的稀硫酸,需要溶质的质量分数为90%的浓硫酸多少克?水多少克?
| 质量分数 | 10% | 20% | 30% | 40% | 50% | 60% | 70% | 80% | 90% | 98% |
| 密度(g/mL) | 1.07 | 1.14 | 1.22 | 1.30 | 1.40 | 1.50 | 1.61 | 1.73 | 1.80 | 1.84 |
(2)质量分数80%和20%的两种硫酸溶液等体积混合后,溶液中溶质的质量分数是56.2%.(结果保留一位小数)
(3)欲配制300克溶质的质量分数为30%的稀硫酸,需要溶质的质量分数为90%的浓硫酸多少克?水多少克?
3. 烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:
(1)得到沉淀的总质量为9.8g;
(2)该混合溶液中硫酸铜的总质量是多少?
(3)参加反应的NaOH溶液的总质量是多少?
(4)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线.(要求标出具体数值)
 烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g.某同学为测定该混合溶液中硫酸铜的质量,向烧杯中逐渐加入10%的NaOH溶液,得到沉淀的质量记录如下:| 加入NaOH溶液的质量/g | 50.0 | 100.0 | 150.0 | 200.0 | 250.0 |
| 生成沉淀的质量/g | 0.0 | 2.5 | 8.6 | 9.8 | 9.8 |
(2)该混合溶液中硫酸铜的总质量是多少?
(3)参加反应的NaOH溶液的总质量是多少?
(4)画出在该混合溶液中加入NaOH溶液质量与生成沉淀质量变化关系的曲线.(要求标出具体数值)
18.欲除去下列物质中的少量杂质,所用试剂正确的是( )
| 物质 | 杂质 | 试剂 | |
| A | CO2 | SO2 | NaOH溶液 |
| B | KCl溶液 | K2SO4 | Ba(OH)2溶液 |
| C | CO2 | CO | Ca(OH)2溶液 |
| D | CaCO3 | CuSO4 | H2O |
| A. | A | B. | B | C. | C | D. | D |


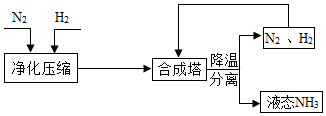 工业上合成 NH 3 的工艺流程可简化为:
工业上合成 NH 3 的工艺流程可简化为:



