题目内容
10.下列除杂的实验过程都不正确的是(括号内为杂质)( )| 选项 | 物 质 | 所选试剂和操作 |
| A | BaSO4(BaCO3) | 加足量稀盐酸、过滤、洗涤、干燥 |
| B | KCl(K2CO3) | 加足量稀硫酸、过滤、蒸发、结晶 |
| C | CuO(Cu) | 在空气中充分灼烧 |
| D | CO(HCl气体) | 足量的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答 解:A、BaCO3能与足量稀盐酸反应生成氯化钡、水和二氧化碳,硫酸钡不与稀盐酸反应,再过滤、洗涤、干燥,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
B、K2CO3能与足量稀硫酸反应生成硫酸钾、水和二氧化碳,能除去杂质但引入了新的杂质硫酸钾,不符合除杂原则,故选项所采取的方法错误.
C、Cu在空气中充分灼烧生成氧化铜,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
D、HCl气体能与NaOH溶液反应生成氯化钠和水,一氧化碳不与NaOH溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确.
故选:B.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
相关题目
1.如图化学反应的颜色变化体现了“魔法世界,魅力化学”,其中X可能是( )


| A. | HCl | B. | H2SO4 | C. | NaOH | D. | Ca(OH)2 |
18.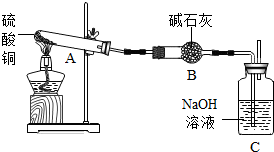 已知:①一定温度下,硫酸铜受热分解生成CuO、SO3、SO2、O2;②SO3、SO2都能被碱石灰和氢氧化钠溶液吸收.利用如图所示装置加热10.0g硫酸铜粉末直至完全分解,各装置的质量变化关系如表所示:
已知:①一定温度下,硫酸铜受热分解生成CuO、SO3、SO2、O2;②SO3、SO2都能被碱石灰和氢氧化钠溶液吸收.利用如图所示装置加热10.0g硫酸铜粉末直至完全分解,各装置的质量变化关系如表所示:
该实验条件下,硫酸铜分解的化学方程式是 ( )
 已知:①一定温度下,硫酸铜受热分解生成CuO、SO3、SO2、O2;②SO3、SO2都能被碱石灰和氢氧化钠溶液吸收.利用如图所示装置加热10.0g硫酸铜粉末直至完全分解,各装置的质量变化关系如表所示:
已知:①一定温度下,硫酸铜受热分解生成CuO、SO3、SO2、O2;②SO3、SO2都能被碱石灰和氢氧化钠溶液吸收.利用如图所示装置加热10.0g硫酸铜粉末直至完全分解,各装置的质量变化关系如表所示:| 装置 | A(试管+粉末) | B | C |
| 反应前质量/g | 42.0 | 75.0 | 140.0 |
| 反应后质量/g | 37.0 | 79.5 | 140.0 |
| A. | 4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑ | |
| B. | 3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ | |
| C. | 5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ | |
| D. | 6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑ |
5.下列关于物质在氧气中燃烧现象的描述错误的是( )
| A. | 木炭在氧气中燃烧,有黑烟生成 | |
| B. | 细铁丝在氧气中燃烧,有黑色固体生成 | |
| C. | 蜡烛在氧气中燃烧,瓶壁有水雾生成 | |
| D. | 白磷在氧气中燃烧,有大量白烟生成 |
15.下列类推正确的是( )
| A. | 某有机物燃烧生成二氧化碳和水,则该物质中一定含有碳、氢、氧三种元素 | |
| B. | 向某固体中滴加稀盐酸,有无色气泡生成,则该固体中一定含有CO32- | |
| C. | 单质是由同种元素组成的,则由同种元素组成的物质就是单质 | |
| D. | 酸性溶液的pH小于7,则pH小于7的溶液一定显酸性 |
2.将密封良好充有氮气的方便面从平原带到高原时,包装会鼓起,袋内气体分子( )
| A. | 间隔变大 | B. | 质量增大 | C. | 体积增大 | D. | 数目增多 |
19.下列变化属于物理变化的是( )
| A. | 食物腐烂 | B. | 铁锅生锈 | C. | 纸张燃烧 | D. | 剪纸成花 |