题目内容
18.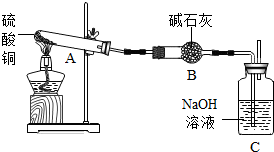 已知:①一定温度下,硫酸铜受热分解生成CuO、SO3、SO2、O2;②SO3、SO2都能被碱石灰和氢氧化钠溶液吸收.利用如图所示装置加热10.0g硫酸铜粉末直至完全分解,各装置的质量变化关系如表所示:
已知:①一定温度下,硫酸铜受热分解生成CuO、SO3、SO2、O2;②SO3、SO2都能被碱石灰和氢氧化钠溶液吸收.利用如图所示装置加热10.0g硫酸铜粉末直至完全分解,各装置的质量变化关系如表所示:| 装置 | A(试管+粉末) | B | C |
| 反应前质量/g | 42.0 | 75.0 | 140.0 |
| 反应后质量/g | 37.0 | 79.5 | 140.0 |
| A. | 4CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$4CuO+2SO3↑+2SO2↑+O2↑ | |
| B. | 3CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$3CuO+SO3↑+2SO2↑+O2↑ | |
| C. | 5CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$5CuO+SO3↑+4SO2↑+2O2↑ | |
| D. | 6CuSO4$\frac{\underline{\;\;△\;\;}}{\;}$6CuO+4SO3↑+2SO2↑+O2↑ |
分析 根据C装置中数据可知,碱石灰完全吸收了二氧化硫和三氧化硫,然后根据质量守恒定律分析每个装置的质量变化情况,从而分析反应中各物质的质量.
解答 解:根据质量守恒定律分析,反应生成气体的质量为42.0g-37.0g=5g,生成氧化铜的质量为10g-5g=5g;干燥管完全吸收了二氧化硫和三氧化硫,其质量为79.5g-75g=4.5g,生成的氧气的质量为5g-4.5g=0.5g;则参加反应的硫酸铜和生成氧化铜及生成的氧气的质量比为10g:5g:0.5g=20:10:1,表现在化学方程式中的化学计量数之比为:$\frac{20}{160}$:$\frac{10}{80}$:$\frac{1}{32}$=4:4:1,
从题干中可以看出,只有A答案符合这个比例.
故选:A.
点评 本题着重考查了质量守恒定律的应用,解题的关键根据装置的质量差分析出各物质的质量,然后求出方程式中物质的化学计量数.

练习册系列答案
相关题目
8.除了对汽车尾气的检测,还有哪些措施对PM2.5的治理不能起到积极作用( )
| A. | 减少火力发电,提倡使用水能、太阳能发电 | |
| B. | 积极植树造林,防治扬尘污染 | |
| C. | 植树造林控制扬尘 | |
| D. | 停车时候把空调稍微调低一点 |
6.下列叙述中,错误的是( )
| A. | 铵态氮肥不能与草木灰(主要成分是碳酸钾)混合施用 | |
| B. | 在煤中加入石灰石和生石灰作固硫剂以减少空气污染 | |
| C. | 在图书档案、贵重设备、精密仪器等发生火灾时,可用泡沫灭火器扑灭 | |
| D. | 含碳酸氢钠的药物可以治疗胃酸过多症 |
3.如图为甲、乙两种固体物质的溶解度曲线,下列叙述不正确的是( )
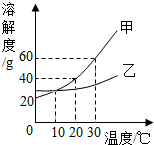

| A. | 甲、乙两种物质均属于易溶物质 | |
| B. | 甲物质的溶液度受温度变化的影响较大 | |
| C. | 在20℃时,甲、乙两种物质的饱和溶液中溶质的质量相等 | |
| D. | 当甲中含有少量的乙时,可用降温结晶法提纯 |
10.下列除杂的实验过程都不正确的是(括号内为杂质)( )
| 选项 | 物 质 | 所选试剂和操作 |
| A | BaSO4(BaCO3) | 加足量稀盐酸、过滤、洗涤、干燥 |
| B | KCl(K2CO3) | 加足量稀硫酸、过滤、蒸发、结晶 |
| C | CuO(Cu) | 在空气中充分灼烧 |
| D | CO(HCl气体) | 足量的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
7.以下是四位同学对某物质的正确判断,请根据他们的讨论推断该物质是( )


| A. | CH4 | B. | CO | C. | C2H5OH | D. | H2 |
3.下列属于空气污染物的是( )
| A. | 一氧化碳 | B. | 二氧化碳 | C. | 氧气 | D. | 氮气 |