题目内容
20.在电缆生产过程中会产生一定量的含铜废料.据报道,在通入空气并加热的条件下,铜与稀硫酸反应转化为硫酸铜,该反应的化学方程式为:2Cu+2H2SO4+O2 $\frac{\underline{\;\;△\;\;}}{\;}$ 2CuSO4+2H2O.若用一定量溶质的质量分数为9.8%的稀硫酸恰好处理2000g含铜3.2%的废料(假设其他杂质不和硫酸反应且不溶于水),计算:(1)2000g含铜3.2%的废料中含铜的质量64g
(2)反应后所得硫酸铜溶液中溶质的质量分数.
分析 依据废料中铜的含量可以求出铜的质量,根据铜的质量利用方程式的物质间量的关系分析解答即可.
解答 解:(1)废料中含铜的质量是2000g×3.2%=64g,故填:64;
(2)设需硫酸的质量为x,参加反应氧气的质量为y,生成硫酸铜的质量为z
2Cu+2H2SO4+O2 $\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O
128 196 32 320
64 g x y z
$\frac{128}{64g}=\frac{196}{x}=\frac{32}{y}=\frac{320}{z}$
x=98 g y=16 g z=160 g
则反应的硫酸溶液的质量是$\frac{98g}{9.8%}$=1000g
故所得溶液的质量分数为$\frac{160g}{64g+1000g+16g}$×100%=14.8%
答:反应后所得硫酸铜溶液中溶质的质量分数为14.8%.
点评 本题主要考查学生运用化学方程式和溶质质量分数公式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
8.除了对汽车尾气的检测,还有哪些措施对PM2.5的治理不能起到积极作用( )
| A. | 减少火力发电,提倡使用水能、太阳能发电 | |
| B. | 积极植树造林,防治扬尘污染 | |
| C. | 植树造林控制扬尘 | |
| D. | 停车时候把空调稍微调低一点 |
5.下列属于物理变化的是( )
| A. | 用鲜奶和乳酸菌制酸牛奶 | B. | 用糯米等原料做甜酿酒 | ||
| C. | 用食醋清洗水壶内的水垢 | D. | 用彩纸折幸运星 |
12.将 50g 98%的浓硫酸全部溶于水配制成 10%的稀硫酸,需要加入水的质量为( )g.
| A. | 400 | B. | 440 | C. | 450 | D. | 500 |
10.下列除杂的实验过程都不正确的是(括号内为杂质)( )
| 选项 | 物 质 | 所选试剂和操作 |
| A | BaSO4(BaCO3) | 加足量稀盐酸、过滤、洗涤、干燥 |
| B | KCl(K2CO3) | 加足量稀硫酸、过滤、蒸发、结晶 |
| C | CuO(Cu) | 在空气中充分灼烧 |
| D | CO(HCl气体) | 足量的NaOH溶液 |
| A. | A | B. | B | C. | C | D. | D |
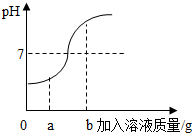 小华同学在用稀硫酸和氢氧化钠溶液进行中和反应实验时,测得反应过程中溶液的酸碱度变化如图所示.
小华同学在用稀硫酸和氢氧化钠溶液进行中和反应实验时,测得反应过程中溶液的酸碱度变化如图所示.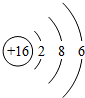 是某粒子的结构示意图,该粒子在化学反应中容易得到(填“得到”或“失去”)电子.
是某粒子的结构示意图,该粒子在化学反应中容易得到(填“得到”或“失去”)电子.