题目内容
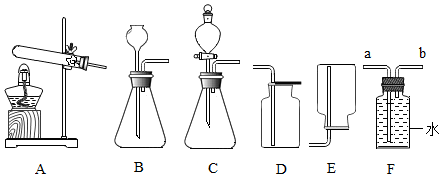
2.小强和几位同学在实验室用如图装置制取几种气体.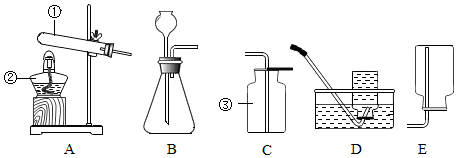
(1)写出仪器名称:①试管 ②酒精灯 ③集气瓶
(2)实验室用高锰酸钾制取氧气时,这个反应的类型属于分解反应,所用的制取装置(也叫发生装置)为A(填图中代号,下同),排水法的收集装置为D.试管口放一团棉花的目的是为了防止高锰酸钾粉末进入导管,用排水法收集完氧气后,先要移出导管,然后再熄灭酒精灯.
(3)实验室利用过氧化氢溶液制取氧气,为了改变此反应的速率需要加入一种黑色固体药品是二氧化锰,它在此反应中起催化作用.反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.实验时所用的制取装置为B,向上排空气法的收集装置为C.
(4)在实验室里若选用B、C装置制取二氧化碳气体,其反应原理可用化学方程式表示为CaCO3+2HCl=CaCl2+H2O+CO2↑.
(5)通过查阅资料得知:氨气(NH3)是一种密度比空气小且极易溶于水的气体,其水溶液称为氨水;小芳用同学加热氯化铵和氢氧化钙的固体混合物制取氨气,她应选择的收集装置是E.
分析 试管是常用的反应容器,酒精灯是常用的加热仪器,集气瓶是收集气体的仪器;制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.氨气(NH3)是一种密度比空气小且极易溶于水的气体,因此只能用向下排空气法收集.
解答 解:(1)试管是常用的反应容器,酒精灯是常用的加热仪器,集气瓶是收集气体的仪器,故答案为:试管;酒精灯;集气瓶;
(2)如果用高锰酸钾制氧气就需要加热,高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,属于分解反应;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;验结束应先移出导管,后熄灭酒精灯,其原因是:防止水倒流,使试管炸裂;故答案为:分解;A;D;为了防止高锰酸钾粉末进入导管;移出导管;熄灭酒精灯;
(3)如果用双氧水和二氧化锰制氧气就不需要加热,其中二氧化锰起催化作用;过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;故答案为:二氧化锰;催化;2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;B;C;
(4)实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热;故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑;
(5)氨气(NH3)是一种密度比空气小且极易溶于水的气体,因此只能用向下排空气法收集;故答案为:E;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写、注意事项和催化剂等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 名校课堂系列答案
名校课堂系列答案| A. | 所有的物质都是由分子构成的 | |
| B. | 气态和液态物质的分子是运动的,固态物质的分子是静止的 | |
| C. | 酸碱中和反应的本质是氢离子和氢氧根离子结合成水分子的过程 | |
| D. | 原子的实际质量很小,等于其含有的质子质量总和 |
| A. | 含有氧元素的化合物叫做氧化物 | |
| B. | 氯化钠的构成粒子是Na+和Cl- | |
| C. | 原子核是由质子和电子构成的 | |
| D. | NH3由一个氮元素和三个氢元素组成 |


 如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题:
如图所示是A、B两种固体物质的溶解度曲线,请回答下列问题: