题目内容
5. A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去).
A、B、C、D均含有同一种元素,它们的转化关系如图(部分物质和反应条件已略去).(1)若A是紫红色金属,B为黑色固体,D为难溶性碱,则D的化学式为Cu(OH)2,由C转化为A的化学方程式为CuSO4+Fe=FeSO4+Cu,由B转化为A的化学方程式为H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.
(2)若A属于氧化物,其相对分子质量为56,A与水化合得B,C是白色难溶固体,则B的俗称是消石灰或熟石灰,由B转化为C的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
分析 (1)根据“A是紫红色金属”,所以A是铜,根据“A、B、C、D均含有同一种元素”,“D为难溶性碱”,所以D是氢氧化铜,由于C能够和氢氧化铜相互转化,且C能够转化为铜,所以C是铜的盐溶液,如硫酸铜、氯化铜等,依据转化关系可知,B应该为氧化铜,然后代入转化关系中验证即可;
(2)根据“A属于氧化物,其相对分子质量为56”,所以A为氧化钙;根据“A与水化合得B”,所以B是氢氧化钙,C是“白色难溶固体”,所以C是碳酸钙,D和碳酸钙能相互转化,D可以是钙盐,也可以是二氧化碳,然后将推出的各种物质代入转化关系中验证即可;
(3)根据反应满足的条件结合方程式的书写规则写出方程式.
解答 解:(1)根据“A是紫红色金属”,所以A是铜,根据“A、B、C、D均含有同一种元素”,“D为难溶性碱”,所以D是氢氧化铜,由于C能够和氢氧化铜相互转化,且C能够转化为铜,所以C是铜的盐溶液,如硫酸铜、氯化铜等,依据转化关系可知,B应该为氧化铜,经过验证推出的各种物质均满足题中的转化关系,所以D的化学式为:Cu(OH)2;由C转化为A的化学方程式为CuSO4+Fe=FeSO4+Cu,由B转化为A的化学方程式为H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O;
(2)根据“A属于氧化物,其相对分子质量为56”,所以A为氧化钙;根据“A与水化合得B”,所以B是氢氧化钙,C是“白色难溶固体”,所以C是碳酸钙,D和碳酸钙能相互转化,D可以是钙盐,也可以是二氧化碳,经过验证推出的各种物质均满足题中的转化关系.则B的俗称为氢氧化钙,可以用于改良酸性土壤;由B转化为C的化学方程式为Ca(OH)2+CO2═CaCO3↓+H2O.
故答案为:
(1)Cu(OH)2;CuSO4+Fe=FeSO4+Cu; H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O (或CO、C)
(2)消石灰或熟石灰;Ca(OH)2+Na2CO3═CaCO3↓+2NaOH或Ca(OH)2+CO2═CaCO3↓+H2O
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案| A. | BaSO4、NaOH、HCl | B. | AgNO3、HCl、KNO3 | ||
| C. | CuSO4、KCl、H2SO4 | D. | Na2CO3、NaCl、Na2SO4 |
| A. |  塑料盆 | B. |  羊毛衫 | C. |  玻璃杯 | D. |  不锈钢刀具 |
【提出问题】为什么会生成淡黄色固体?
【查阅资料】小光查阅资料,记录了下列几种物质的颜色:
| 物质 | MgO | MgCl2 | Mg3N2 | Mg(NO3)2 | MgCO3 | Mg(OH)2 |
| 颜色 | 白色 | 白色 | 淡黄色 | 白色 | 白色 | 白色 |
【提出猜想】分析资料:小光认为淡黄色固体可能是由镁与空气中的氮气(或N2)反应生成的;
【实验探究】小光设计实验证实了自己的猜想,他的方案可能是将点燃的镁条伸人充满氮气的集气瓶中,观察是否生成淡黄色的固体.
【实验结论】根据小光的实验结果,写出镁条在空气中燃烧时发生的两个反应的化学方程2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO、3Mg+N2$\frac{\underline{\;点燃\;}}{\;}$Mg3N2;
【反思与评价】通过上述实验,你对燃烧的认识燃烧不一定要有氧气参加.
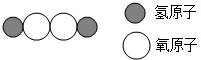
| A. | 它是由氢气和氧气组成的 | B. | 它是由氢分子和氧分子构成的 | ||
| C. | 它是由氢元素和氧元素组成 | D. | 它是由2个氢原子和2个氧原子构成 |