题目内容
9.下列各组溶液,不用其他试剂无法鉴别的是( )| A. | Na2CO3 H2SO4 BaCl2 HCl | B. | HCl NaOH BaCl2 MgSO4 | ||
| C. | Na2CO3 HCl H2SO4 KOH | D. | HCl NaOH CuSO4 NaNO3 |
分析 在不另加试剂就能鉴别的题目中,首先观察有无有特殊颜色的物质,若有,将有颜色的溶液鉴别出来,然后再借用这种溶液鉴别其它溶液把其它没有确定出的物质确定出来;若都没有颜色就将溶液两两混合,根据混合后的现象进行分析鉴别.
解答 解:A、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现一次白色沉淀和一次放出气体,该溶液为碳酸钠溶液;与碳酸钠溶液产生气体的溶液为HCl、H2SO4,产生白色沉淀的为氯化钡;与氯化钡溶液混合产生白色沉淀的为硫酸溶液;故不加其他试剂可以鉴别.
B、组内四种物质的溶液两两混合时,其中有一种溶液与其它三种溶液混合时出现2次白色沉淀,该溶液为MgSO4溶液;与MgSO4溶液产生白色沉淀的溶液为NaOH、BaCl2,剩余的溶液为稀盐酸;再将稀盐酸分别滴加至两种白色沉淀中,沉淀消失的原溶液为氢氧化钠溶液,无明显变化的原溶液是氯化钡溶液;故不加其他试剂可以鉴别.
C、Na2CO3溶液与稀硫酸、稀盐酸反应均能产生气体,但其余两两混合均没有明显现象,故不加其他试剂无法鉴别.
D、CuSO4溶液是蓝色的,能与CuSO4溶液反应产生蓝色沉淀的是的是NaOH溶液,再将剩余的两种溶液分别电滴加至蓝色沉淀中,能使沉淀消失的是稀盐酸,无明显变化的是NaNO3溶液,故不加其他试剂可以鉴别.
故选:C.
点评 解答不另加试剂就能鉴别的题目时,若选项中有带色的离子,首先鉴别,然后再鉴别其它的物质;若都没有颜色,可将溶液两两混合,根据混合后的现象进行鉴别.

练习册系列答案
相关题目
19.大理石广泛存在于自然界,某种大理石除主要成分CaC03外,还有少量的硫化钙.甲和乙两位同学用这种大理石和稀盐酸反应分别并展以下探究.
【查阅资料】资料一:在常温下,测的浓度均为a%的下列5种溶液的pH大小情况:
A.H2S04+2NaHC03═Na2S04+2H20+2C02↑ B.2HCl+CaS═CaCl2+H2S↑
C.C02+H20+Ca(C10)2═CaC03↓+2HClO D.H2S+CuS04═H2S04+CuS↓
资料二:常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰
【实验探究】同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:
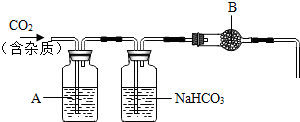
(1)制备的C02气体中,可能含有的杂质是HCl、H2S、和水蒸气;
(2)上述装置中,A是硫酸铜溶液,饱和NaHCO3溶液可以吸收HCl、H2S等酸性气体;
(3)上述装置中,B物质可能是无水氯化钙(写名称);
(4)用这个实验得到的气体测定C02的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”);
(5)乙同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
乙同学通过分析计算,得出结论:该实验中生成的二氧化碳的质量是4.4g,大理石样品纯度为83.3%.请你评价他的结论是否正确错误(填“正确”或“错误”,并简述理由)大理石中含有硫化物,硫化物与盐酸反应会生成硫化氢气体逸出,把生成的气体全部作为二氧化碳,使碳酸钙质量偏大,造成质量分数偏大.
【查阅资料】资料一:在常温下,测的浓度均为a%的下列5种溶液的pH大小情况:
| 溶质 | H2S04 | HCl | H2S | H2C03 | HClO |
| PH | 小→大 | ||||
C.C02+H20+Ca(C10)2═CaC03↓+2HClO D.H2S+CuS04═H2S04+CuS↓
资料二:常见干燥剂有①浓硫酸②无水氯化钙③碱石灰④生石灰
【实验探究】同学为了得到纯净的二氧化碳,设计了如下装置,请你分析:

(1)制备的C02气体中,可能含有的杂质是HCl、H2S、和水蒸气;
(2)上述装置中,A是硫酸铜溶液,饱和NaHCO3溶液可以吸收HCl、H2S等酸性气体;
(3)上述装置中,B物质可能是无水氯化钙(写名称);
(4)用这个实验得到的气体测定C02的相对分子质量,如果B物质失效,测定结果偏高(填“偏高”、“偏低”或“不受影响”);
(5)乙同学为了计算这种大理石中含碳酸钙质量分数,进行了如下定量实验:
| 实验步骤 | I.将适量盐酸加入烧杯中并称重 | Ⅱ.称取少量大理石样品加入烧杯中,使之与过量稀盐酸反应 | Ⅲ.待反应完全后,称重 |
| 实验图示 |  | ||
| 实验数据 | 烧杯和盐酸的质量为100.0g | 大理石样品的质量为12.0g | 烧杯和其中混合物的质量为107.6g |
20.下来有关环境问题的叙述正确的是( )
| A. | 为解决“白色污染”问题,可将废弃塑料焚烧处理 | |
| B. | 汽车使用乙醇汽油可减缓温室效应 | |
| C. | 通过秸秆综合利用,杜绝露天焚烧,来降低空气中PM2.5的含量 | |
| D. | 化工厂通过加高烟囱来排放废弃,以防止形成酸雨 |
19.下列实验方案设计不合理的是( )
| A. | 鉴别铁粉和木炭粉:观察颜色 | |
| B. | 鉴别羊毛和合成纤维:灼烧、闻气味 | |
| C. | 除去铜中混有的氧化铜:加过量稀硫酸,过滤 | |
| D. | 除去氧化钙中混有的碳酸钙:高温煅烧 |