题目内容
14.海洋中蕴藏着丰富的化学资源,如NaCl、KCl、Na2SO4、MgCl2、CaCl2等物质.从海水中提取金属镁的主要流程如下: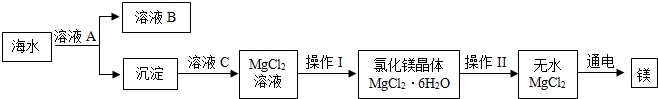
(1)将海水中的镁提取出来,首先要让海水中的镁离子形成沉淀而富集起来.为了使镁离子尽可能多地转化成为沉淀,应加入的溶液A中溶质可能是Ca(OH)2(填化学式),发生化学反应方程式为MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓.
(2)已知MgCl2的溶解度随温度升高而增大,且氯化镁晶体(MgCl2•6H2O)在受热情况下容易分解产生Mg(OH)Cl以及另外两种产物,请写出发生的化学反应方程式为MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)Cl+HCl↑+5H2O↑.请补充完整操作的操作过程:蒸发浓缩、降温结晶、过滤.
(3)电解熔融的无水MgCl2可以得到金属镁.该反应的化学反应方程式为MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑,属于基本反应类型中的分解反应.
分析 (1)氯化镁转化为氢氧化镁需要加入碱液,将MgCl2完全转化为Mg(OH)2;
(2)根据反应的原理以及分离氯化镁的方法来分析;
(3)无水MgCl2电解制取Mg,同时生成氯气,写出反应的化学方程式即可.
解答 解:(1)氯化镁转化为氢氧化镁需要加入碱液以提供氢氧根,此处选择过量的Ca(OH)2溶液进行反应,生成氯化钙和氢氧化镁;故填:Ca(OH)2;MgCl2+Ca(OH)2=CaCl2+Mg(OH)2↓;
(2)氯化镁晶体(MgCl2•6H2O)在受热情况下容易分解产生Mg(OH)Cl以及氯化氢和水蒸气;因为MgCl2的溶解度随温度升高而增大,所以得到氯化镁晶体应采取蒸发浓缩、降温结晶和过滤的方法;故填:MgCl2•6H2O$\frac{\underline{\;\;△\;\;}}{\;}$Mg(OH)Cl+HCl↑+5H2O↑;降温结晶;过滤;
(3)无水MgCl2电解制取Mg,同时生成氯气,反应的化学方程式为:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑.该反应是由一种物质反应生成两种污渍,符合一变多的特征,属于分解反应;故填:MgCl2$\frac{\underline{\;通电\;}}{\;}$Mg+Cl2↑;分解.
点评 本题难度不大,明确工业上制取金属镁的反应流程、碱的化学性质、化学方程式的书写方法等是正确解答本题的关键.

练习册系列答案
相关题目
4.10克20%的氢氧化钠溶液和10克20%的稀硫酸充分混合,混合后的溶液与下列物质不能发生反应的是( )
| A. | 铁 | B. | 氯化钡溶液 | C. | 硫酸铜溶液 | D. | 氧化铜 |
9.下列各组溶液,不用其他试剂无法鉴别的是( )
| A. | Na2CO3 H2SO4 BaCl2 HCl | B. | HCl NaOH BaCl2 MgSO4 | ||
| C. | Na2CO3 HCl H2SO4 KOH | D. | HCl NaOH CuSO4 NaNO3 |
19.下列做法会损害人体健康的是( )
| A. | 用含小苏打的发酵粉焙制糕点 | B. | 用食醋除去松花蛋的涩味 | ||
| C. | 用霉变花生压榨成花生油食用 | D. | 氮气充入食品包装袋内防腐 |
4.下列物质由离子构成的是( )
| A. | 氨 | B. | 金刚石 | C. | 二氧化碳 | D. | 氯化钠 |

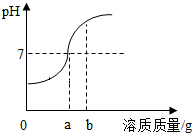 用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的pH变化如图所示
用稀硫酸和氢氧化钠溶液进行中和反应的实验时,反应过程中溶液的pH变化如图所示