题目内容
4.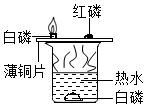 如图是探究燃烧条件的实验装置图,已知白磷和红磷的着火点分别是40℃、240℃.回答下列问题:
如图是探究燃烧条件的实验装置图,已知白磷和红磷的着火点分别是40℃、240℃.回答下列问题:(1)该实验主要利用了薄铜片良好的导热性
(2)由薄铜片上的白磷燃烧而红磷不燃烧的事实,说明燃烧需要的条件是温度需要达到着火点
(3)燃着的白磷熄灭后,观察到薄铜片上的白色固体周边的铜片表面变黑,该黑色物质是CuO(填化学式).
分析 (1)根据铜具有导热性解答;
(2)根据燃烧的条件:具有可燃性,温度达到可燃物的着火点,与氧气接触,利用对比实验中的变量分析;
(3)根据铜能与氧气反应生成氧化铜,据此解答.
解答 解:
(1)铜具有良好的导热性,能传递热量,该实验主要利用了薄铜片良好的导热性;
(2)白磷的着火点是40℃,红磷的着火点是240℃,薄铜片上的白磷燃烧而红磷不燃烧,说明物质燃烧,温度需要达到着火点;
(3)铜片表面变黑是因为铜与氧气反应生成了氧化铜,故填:CuO;
答案:
(1)导热;
(2)温度需要达到着火点;
(3)CuO.
点评 本题考查的是燃烧的条件的实验测定,完成此题,可以依据已有的知识进行.解答本题关键是要熟悉燃烧的条件,知道对照实验的设计方法,只允许有一个变量.

练习册系列答案
相关题目
13.植物光合作用可表示为:二氧化碳+水$\stackrel{光照}{→}$淀粉+氧气.根据以上信息,下列关于淀粉组成的说法中正确的是( )
| A. | 只含碳、氢元素 | B. | 含有碳、氢、氧三种元素 | ||
| C. | 含有碳、氢元素,可能含有氧元素 | D. | 含三种以上的元素 |
10.与元素化学性质最密切的是( )
| A. | 原子核内质子数 | B. | 原子的最外层电子数 | ||
| C. | 元素的核电荷数 | D. | 元素的相对原子质量 |
17. 听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟.查阅资料,墨鱼骨含碳酸钙80%~85%以上,还含有多种氨基酸.墨鱼骨能治疗胃酸过多的原因是:CaCO3+2HCl═CaCl2+H2O+CO2↑(用化学方程式表示).为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究.
听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟.查阅资料,墨鱼骨含碳酸钙80%~85%以上,还含有多种氨基酸.墨鱼骨能治疗胃酸过多的原因是:CaCO3+2HCl═CaCl2+H2O+CO2↑(用化学方程式表示).为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究.
(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克.处理如下:
CO2质量=10克-5.4克=4.6克
设碳酸钙质量为M
CaCO3$\frac{\underline{\;高温\;}}{\;}$CO2↑+CaO
100 44
M 4.6克
$\frac{100}{M}$=$\frac{44}{4.6克}$ 所以M=10.5克
CaCO3%=$\frac{10.5克}{10克}$×100%=105%
小科的计算结果与事实不符,产生错误的原因是:墨鱼骨还含有多种氨基酸,高温灼烧时导致氨基酸受热分解碳化.
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是除去二氧化碳中混有的水蒸气,从而减少测量误差.
(3)小妍将30mL稀盐酸分3次加入到3克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不
再变化时,读出水的体积,结果见上表.已知本实验条件下CO2的密度为2.0克/升,求:该墨鱼骨粉样品中CaCO3的质量分数.
 听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟.查阅资料,墨鱼骨含碳酸钙80%~85%以上,还含有多种氨基酸.墨鱼骨能治疗胃酸过多的原因是:CaCO3+2HCl═CaCl2+H2O+CO2↑(用化学方程式表示).为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究.
听说墨鱼骨能治疗胃酸过多,好学的小科和小妍想探个究竟.查阅资料,墨鱼骨含碳酸钙80%~85%以上,还含有多种氨基酸.墨鱼骨能治疗胃酸过多的原因是:CaCO3+2HCl═CaCl2+H2O+CO2↑(用化学方程式表示).为了测定墨鱼骨中碳酸钙的含量,他们先将墨鱼骨洗净晒干,并按各自设计实验方法进行研究.(1)小科称取10克洗净晒干的墨鱼骨,高温灼烧至质量不变,冷却后称得剩余固体质量为5.4克.处理如下:
CO2质量=10克-5.4克=4.6克
设碳酸钙质量为M
CaCO3$\frac{\underline{\;高温\;}}{\;}$CO2↑+CaO
100 44
M 4.6克
$\frac{100}{M}$=$\frac{44}{4.6克}$ 所以M=10.5克
CaCO3%=$\frac{10.5克}{10克}$×100%=105%
小科的计算结果与事实不符,产生错误的原因是:墨鱼骨还含有多种氨基酸,高温灼烧时导致氨基酸受热分解碳化.
(2)小研用如图所示的实验装置进行实验,其中浓硫酸的作用是除去二氧化碳中混有的水蒸气,从而减少测量误差.
(3)小妍将30mL稀盐酸分3次加入到3克样品中,每次加入盐酸后充分反应,待量筒内的水的体积不
| 第一次 | 第二次 | 第三次 | |
| 加入稀盐酸的体积(毫升) | 10 | 10 | 10 |
| 进入量筒内水的体积(毫升) | 220 | 220 | 110 |
14. 食盐是生活和工农业生产中最常见的物质之一.晒盐场利用晾晒海水得到粗盐和卤水.
食盐是生活和工农业生产中最常见的物质之一.晒盐场利用晾晒海水得到粗盐和卤水.
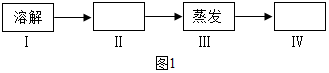
(1)去除粗盐中难溶性的杂质,主要步骤有:溶解、过滤、蒸发;在过滤操作中,玻璃棒的作用是引流.
(2)在20℃时,向4个盛有200g水的烧杯中,分别加入一定质量的纯净氯化钠固体,并充分搅拌,4组实验数据记录如下
以下是关于上述实验的叙述,正确的是ABC(填写序号).
A.①②所得溶液是不饱和溶液 B.③④所得溶液中,溶液的质量分数相等
C.20℃时,200g水中最多可溶解氯化钠的质量为72g
D.20℃时,将④继续恒温蒸发100g水,过滤,得到质量为36g的固体
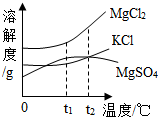
(3)卤水的主要成分及其溶解度曲线如图,t1℃时,将3种图中物质的饱和溶液升温到t2℃,3种溶液溶质的质量分数由小到大的顺序是KCl<MgSO4<MgCl2.
 食盐是生活和工农业生产中最常见的物质之一.晒盐场利用晾晒海水得到粗盐和卤水.
食盐是生活和工农业生产中最常见的物质之一.晒盐场利用晾晒海水得到粗盐和卤水.(1)去除粗盐中难溶性的杂质,主要步骤有:溶解、过滤、蒸发;在过滤操作中,玻璃棒的作用是引流.
(2)在20℃时,向4个盛有200g水的烧杯中,分别加入一定质量的纯净氯化钠固体,并充分搅拌,4组实验数据记录如下
| 实验序号 | ① | ② | ③ | ④ |
| 加入氯化钠的质量/g | 9 | 36 | 81 | 90 |
| 所得溶液的质量/g | 209 | 236 | 272 | 272 |
A.①②所得溶液是不饱和溶液 B.③④所得溶液中,溶液的质量分数相等
C.20℃时,200g水中最多可溶解氯化钠的质量为72g
D.20℃时,将④继续恒温蒸发100g水,过滤,得到质量为36g的固体
(3)卤水的主要成分及其溶解度曲线如图,t1℃时,将3种图中物质的饱和溶液升温到t2℃,3种溶液溶质的质量分数由小到大的顺序是KCl<MgSO4<MgCl2.