题目内容
6.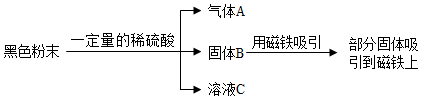 取含有铁粉、氧化铜、银粉(黑色)三种物质组成的黑色粉末进行实验,流程如图:
取含有铁粉、氧化铜、银粉(黑色)三种物质组成的黑色粉末进行实验,流程如图:(1)生成气体A的化学反应方程式为Fe+H2SO4═FeSO4+H2↑;
(2)固体B中的金属有Fe、Cu、Ag;
(3)溶液C中的溶质是FeSO4.
分析 根据取含有铁粉、氧化铜、银粉(黑色)三种物质组成的黑色粉末进行实验,加入一定量的稀硫酸,生成气体,说明铁与稀硫酸反应生成氢气和硫酸亚铁;而氧化铜与稀硫酸反应生成硫酸铜溶液和水;用磁铁吸引后,部分被吸引,说明有剩余铁,故硫酸铜溶液完全与铁反应生成铜和硫酸亚铁,故推测固体B、溶液C中的物质.
解答 解:根据取含有铁粉、氧化铜、银粉(黑色)三种物质组成的黑色粉末进行实验,加入一定量的稀硫酸,生成气体,说明铁与稀硫酸反应生成氢气和硫酸亚铁;而氧化铜与稀硫酸反应生成硫酸铜溶液和水;用磁铁吸引后,部分被吸引,说明有剩余铁,故硫酸铜溶液完全与铁反应生成铜和硫酸亚铁,故推测固体B为铁、铜、银,溶液C中的物质为硫酸亚铁.
故答案为:
Fe+H2SO4═FeSO4+H2↑;Fe、Cu、Ag;FeSO4;
点评 做化学推断题的步骤方法:①审题;②分析:抓住关键,找准解题的突破口;③解答:按照分析和推理的结果,进行认真而全面的解答;④检验:得出结论后切勿忘记验证.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.氢氧化钠是一种重要的碱,同学们对它进行了如下探究:
实验探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全反应. 下列实验方案中,不正确的是方案一、三.
实验探究二:一瓶长期敞口放置的氢氧化钠溶液是否变质.
【査阅资料】氯化钡溶液显中性
【提出猜想】
猜想一:该溶液没有变质.
猜想二:该溶液部分变质.
猜想三:该溶液完全变质.
【实验探究】
【讨论交流】
(1)在上述实验探究中,小芳同学提出实验步骤一中的氯化钡溶液用适量氢氧化钡溶液代替也可得出猜想二成立的结论.你认为小芳的方案不可行(填“可行”或“不可行”),理由是氢氧化钡和碳酸钠反应生成氢氧化钠,氢氧化钠溶液能使酚酞试液变红色.
(2)这瓶长期敞口放置的氢氧化钠溶液变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示),除去已部分变质的氢氧化钠中的杂质,可以选用的试剂是C(填字母序号).
A.氯化钙溶液 B.盐酸 C.氢氧化钙溶液 D.MgCl2溶液.
实验探究一:判断氢氧化钠溶液与稀盐酸混合后是否恰好完全反应. 下列实验方案中,不正确的是方案一、三.
| 实验步骤 | 实验现象预测 | 结论 | |
| 方案一 | 取少量反应后的溶液于一支试管中.滴加几滴无色酚酞试液,振荡 | 酚酞试液不变色 | 恰好完全反应 |
| 方案二 | 用一根洁净的玻璃棒蘸取反应后的溶液沾在pH试纸上,与标准比色卡对照 | pH=7 | 恰好完全反应 |
| 方案三 | 取少量反应后的溶液于一支试管中,滴加硝酸银溶液 | 有白色沉淀产生 | 盐酸过量,没有 恰好完全反应 |
【査阅资料】氯化钡溶液显中性
【提出猜想】
猜想一:该溶液没有变质.
猜想二:该溶液部分变质.
猜想三:该溶液完全变质.
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 步骤一:取少量该溶液于试管中,向其中滴加过量的氯化钡溶液 | 生成白色沉淀 | 猜想一不成立 |
| 步骤二:静止,取步骤一充分反应后的上层淸液于另一支试管中,滴加酚酞溶液.振荡 | 溶液变红色 | 由实验步骤一和步骤二的现象得出猜想二成立 |
(1)在上述实验探究中,小芳同学提出实验步骤一中的氯化钡溶液用适量氢氧化钡溶液代替也可得出猜想二成立的结论.你认为小芳的方案不可行(填“可行”或“不可行”),理由是氢氧化钡和碳酸钠反应生成氢氧化钠,氢氧化钠溶液能使酚酞试液变红色.
(2)这瓶长期敞口放置的氢氧化钠溶液变质的原因是2NaOH+CO2═Na2CO3+H2O(用化学方程式表示),除去已部分变质的氢氧化钠中的杂质,可以选用的试剂是C(填字母序号).
A.氯化钙溶液 B.盐酸 C.氢氧化钙溶液 D.MgCl2溶液.
14.向一定质量的硝酸银和硝酸铜的混合溶液中加入m克锌粉,充分反应后过滤,将滤渣洗涤、干燥后称量,得到的固体质量为m克,据此,下列说法不正确的是( )
| A. | 滤渣中的物质至少有两种 | |
| B. | 取反应后的滤液观察,滤液可能呈蓝色 | |
| C. | 去反应后的滤液滴加稀盐酸,无白色沉淀产生 | |
| D. | 向滤渣滴加稀盐酸,一定有气泡产生 |
18.在进行了对蜡烛及其燃烧的探究活动后,同学们有如下说法,其中不正确的是( )
| A. | 蜡烛在空气中燃烧时产生明亮的火焰,同时放出较多热量 | |
| B. | 蜡烛燃烧时冒出的黑烟与吹灭蜡烛时产生的白烟是同种物质 | |
| C. | 蜡烛燃烧的生成物主要是水和二氧化碳 | |
| D. | 蜡烛燃烧属于化学变化,其过程中同时有物理变化发生 |
7.区分下列各组物质,所加试剂或操作方法错误的是
( )
| 选项 | 待区分的物质 | 鉴别方法 |
| A | 合成纤维和纯羊毛 | 取样,分别灼烧,并闻气味 |
| B | CaCl2溶液和NaCl溶液 | 取样,分别加入硝酸银溶液,观察是否产生沉淀 |
| C | 稀盐酸和稀硫酸 | 取样,分别AgNO3溶液,观察是否产生沉淀 |
| D | 碳粉和氧化铜 | 取样,分别加入足量稀硫酸,观察是否能溶解 |
| A. | A | B. | B | C. | C | D. | D |
8.下列说法正确的是( )
| A. | 用普通pH试纸测得酸雨的pH=4.8 | |
| B. | 硫在氧气中燃烧,发出淡蓝色的火焰 | |
| C. | 用10 mL量筒量取8mL食盐溶液 | |
| D. | 用燃着的木条鉴别二氧化碳和氮气 |
 ”、“
”、“ ”表示不同种元素的原子.
”表示不同种元素的原子.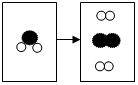
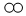 B、
B、 C、
C、